原子与离子的区别
引言
原子是元素的最小单位,由紧密堆积的带正电的原子核和周围带负电的电子组成。原子分为两部分:原子结构和核外区域。原子结构由中性中子(n°)和带正电的质子(P+)组成。在核外区域,存在带负电的电子(e-)。原子以及所有其他元素和化合物都具有质量。构成原子核的质子主要负责其质量的集中。与中子和电子相比,质子质量最大。氢原子在其原子核内有一个质子,周围围绕着一个电子。氢是最轻的元素。每个原子的原子核中都有确定的质子数,这些质子吸引一定数量的电子,使原子呈电中性。可以通过添加或移除电子来产生离子。例如 − 𝐻, 𝑁, 𝑂, 𝐹𝑒。
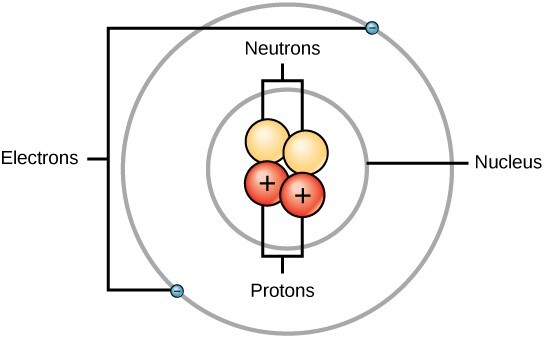
CNX OpenStax, 玻尔原子结构图, CC BY 4.0
构成元素的最小粒子称为原子。质子、中子和电子是亚原子粒子,可以进一步从原子中分离出来,而原子以前被认为是不可破坏的。由于每个原子中的质子和电子数量相等,因此它们都呈电中性。当原子失去或获得电子时,它就会带电。这种带电粒子称为离子。如果获得电子,则带负电,称为阴离子;如果失去电子,则带正电,称为阳离子。原子物理学家对原子外观和行为的最佳解释是现代原子理论。原子理论的基本原理是原子是化学物质的最小组成部分。最基本的化学物质和元素不能进一步发生化学分解。
基于现代原子理论的原子特征
最新或范式化的原子理论称为现代原子理论。现代原子理论是原子物理学家对原子外观和行为的最佳解释。根据原子理论的基本原理,原子是化学物质的最小单位。
最简单的化学物质,不能进一步进行化学分解,称为元素。
与所有其他元素的原子不同,每种元素的原子都是独特的。然而,原子可以进一步分解成亚原子粒子。
质子是原子核中带正电的亚原子粒子,在构成每种元素的每个原子中,其数量相同。
原子核中也包含中子,但它们的数量在同种原子的同位素之间可能不同。
同位素是指中子数不同但质子数相同的原子。例如,所有氢原子都含有一个质子,但该元素有不同的同位素;氢-1不含中子,而氢-2含有一个中子。
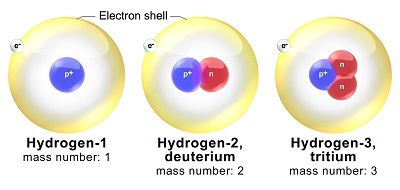
BruceBlaus, Blausen 0530 氢同位素图, CC BY 3.0
此外,围绕带正电原子核的带负电的量子电子受到静电力的吸引。许多原子的基本表示将电子描绘成围绕原子核的球体或粒子,类似于行星绕太阳运行的方式。事实上,这种图示并没有真实或准确地描绘电子的性质。相反,现代原子模型将电子描述为云、波、概率函数,甚至是不确定的。
离子介绍
当原子内质子和电子的分布不平衡时,就会产生离子。离子是最常见的带电粒子类型。离子可以带正电荷,也可以带负电荷。如果原子带电,则称为离子。如果一个原子中的电子比质子多,则称为阴离子。如果一个原子中的质子比电子多,则称为阳离子。它本身可以被解决。当原子获得或失去电子时,就会形成离子。阴离子(-)和阳离子(+)是两种不同类型的离子。
由于原子中质子和电子的数量相等,因此它是电中性的。
然而,在化学反应中,原子试图通过获得或失去一个或多个电子(取决于化合价)来获得稳定的电子构型(电子对或八隅体)。
当原子获得电子时,其电子数量增加;因此,它获得负电荷。
当原子失去电子时,它获得的质子比失去的多,使原子带正电荷。
离子是产生正电荷或负电荷的原子。
当原子失去电子时,我们给它加上“+”号。
当原子获得电子时,我们给它加上“-”号。
原子与离子的区别
| 原子 | 离子 |
|---|---|
| 元素的基本单位。 | 带电的原子或分子。 |
| 质子和电子的比例为1:1。 | 质子和电子的比例不平衡。 |
| 电中性 | 带正电或负电 |
| 它们具有不稳定的价电子层,并且当独立存在时,非常活泼。相反,惰性气体 | 它们的价电子层已完全填充,并且在独立存在的能力方面表现出极好的稳定性。 |
| 可以形成共价键和离子键 | 只有离子键 |
| 分子由原子组成。 | 存在多原子离子和单原子离子。它们也可以形成晶格网络。 |
| 不被电场吸引。 | 取决于离子的电荷,可以被电场吸引 |
结论
从现代原子理论可以得出结论,原子由两部分组成。它们是原子轨道和原子核。原子核由带正电的质子和带中性电荷的中子组成。作为所有事物的基本构成单元,原子构成所有物质。原子可以通过获得或失去电子转变为离子。然而,并非所有离子都是原子,因为一些分子可以通过失去或获得电子转变为离子。原子和离子之间的主要区别在于,前者没有净电荷,而后者有净电荷。
常见问题
1. 所有原子都是离子吗?
从技术上讲,除了惰性气体之外,每个原子都可以形成离子,但并非每个离子都是原子。一些离子可能是多原子的,这意味着它们由原子组组成,例如 $\mathrm{PO^{3-}}$ 磷酸根离子。
2. 离子与其母原子不同吗?
是的,离子的尺寸可能与其母原子的尺寸不同。阴离子大于其母原子,而阳离子通常较小,因为它们失去了外电子层,并且结合得更松散。
3. 离子是否自然存在?
带相反电荷的离子相互吸引,而带相同电荷的离子相互排斥。因此,离子很少单独存在,但有时会与带相反电荷的离子结合形成晶格。人们认为由此产生的化学物质是由离子键结合在一起的,因此它被归类为离子酸。
4. 最小的原子是什么?
已知最小的原子是氦,其半径为31皮米;最大的原子是铯,其半径为298皮米。尽管氢的原子序数小于氦,但其原子半径估计大约大70%。
5. 原子有生命吗?还是惰性的?
不,原子不是生命体。物体是否有生命取决于其是否具有生长、呼吸和繁殖等行为能力。原子无法执行这些功能;只有复杂的结构才能。


 数据结构
数据结构 网络
网络 关系数据库管理系统(RDBMS)
关系数据库管理系统(RDBMS) 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C语言编程
C语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP