晶体和非晶体的区别
引言
物质的基本状态中,分子紧密排列或堆积的是固体。因此,固体分子之间存在强大的吸引力。与其他物质状态相比,固体具有确定的形状和结构刚性。它不像其他状态的气体和液体那样流动或膨胀。因此,在固体的情况下,必须考虑原子的位置而不是移动。这些原子在固体中的排列通常有两种方式。固体中粒子规则重复和有序的排列导致晶体固体的形成。而原子无序和不规则的排列方式形成聚集体则导致非晶态固体的形成。
固体的分类

固体分为两种类型:
晶体固体
非晶态固体
晶体固体进一步分为:
晶体固体
离子晶体
共价晶体
分子晶体
原子晶体
金属晶体
晶体固体
晶体也被称为晶体固体,是一种具有独特内部结构的固体。粒子的排列方式是有序的。因此,晶体固体具有高度有序的微观模式,在各个方向上扩展。对这些结构的研究是晶体学。晶体固体中存在的每种结构在暴露于X射线时都会产生独特的图案。晶体中的对应角度不取决于晶体的大小,而是取决于固体中原子的规则排列。这可以进一步用于检测未知的固体材料。这种类型的离子晶体的断裂导致形成新的晶体,其相交角度与母体晶体相同。
晶体固体进一步分为其他几类,并基于它们存在的分子间吸引力。分子晶体中存在范德华力。在离子晶体中存在离子键。在共价晶体中存在共价键。在金属晶体中存在金属键。在原子晶体中,一个原子与另一个原子键合形成晶体固体。
晶体结构由晶胞区分,它是一个虚构的盒子,包含一个或多个原子,具有独特的空间构型。这些晶胞组合形成晶体的三维排列。这些晶胞的堆积方式使得它们之间没有间隙。晶体中原子的规则排列会导致清晰的熔点和沸点。也就是说,固体原子之间存在的分子间力都相同,并且需要相似的能量来裂解这些分子。具有晶体结构的固体例子有金刚石、食盐、冰、石英、云母、明矾、氟化钙等。晶体中原子的排列如下图所示。
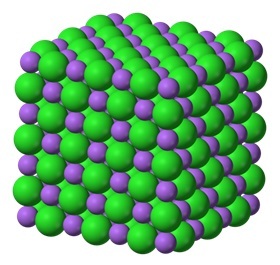
性质
下面详细讨论晶体固体的一些重要性质。
它们具有长程有序。
它们具有明确的熔点。
存在规则排列。
它们是各向异性的,这意味着它们在不同方向上具有不同的特性。
具有三维几何形状。
具有刚性结构。
可以断裂成光滑的表面。
具有恒定的熔化热。
非晶态固体
非晶态固体被称为非晶态固体。这些固体中的原子和分子没有以确定的模式或规则的方式排列。它缺乏晶体固体有序的内部结构。当它们发生断裂时,不会以有序的方式进行,也不会遵循规则的排列。由于它们的原子排列在不同的位置,它们的性质也会随着位置的变化而变化。玻璃是众所周知的非晶态固体的例子,其中原子的排列是不规则的。这就是为什么它们的断裂不遵循任何顺序,即断裂后会得到不同形状的碎片的原因。玻璃看起来像晶体,但这种物质的内部排列非常不同。它们也被称为过冷液体。
非晶态固体有点像液体。由于它们的原子没有以有序的方式排列,这种物质没有确定的形状,它们更像液体。由于其类似液体的特性,它也被称为假固体。这就是为什么玻璃会流动,玻璃制成的窗户在最下部会变厚的原因。
非晶态固体的性质也不同,它不具有任何明确的熔点和沸点。并且物理性质在所有方向上都是相同的,即它们是各向同性的。这是因为原子结合在一起形成聚集体。塑料、橡胶、玻璃、凝胶、聚合物、蜡、润滑剂等都是非晶态固体。
性质
下面讨论非晶态固体的一些重要性质。
它们具有短程有序。
没有明确的熔点。
非晶态固体在高温下加热会转化为类似于晶体的玻璃状材料。
它没有确定的熔化热。
它们是各向同性的,即它们在所有方向上都具有相同的特性。
它可以转化为晶体形式。
它们是固态形式的高粘度过冷液体。
晶体固体和非晶态固体的区别
晶体固体和非晶态固体是两种具有不同性质的固体。因此,即使它们都是固体,它们也是完全不同的材料。这两种固体之间的一些区别在下面的表格中列出。
| 晶体固体 | 非晶态固体 |
|---|---|
| 存在有序排列。 | 不存在这种有序排列。 |
| 它具有明确的熔点。 | 没有明确的熔点。 |
| 各向异性。 | 各向同性。 |
| 存在长程有序。 | 只有短程有序。 |
| 包含共价键、离子键、范德华力和金属键。 | 仅包含共价键。 |
| 具有明确的熔化热。 | 没有明确的熔化热。 |
| 假固体。 | 真固体。 |
| 对称。 | 不对称。 |
| 具有确定的形状。 | 没有确定的形状。 |
| 例如氯化钠、金刚石、石英等。 | 例如玻璃、聚合物、蜡等。 |

结论
固体是一种化学状态,其中粒子以一种原子紧挨着另一种原子的方式排列。它们具有确定的形状和大小。并且不会随着任何外部压力而变化。固体通常分为两种类型:晶体固体和非晶态固体。原子具有由粒子或原子规则周期性排列形成的三维几何形状的固体是晶体固体。而不包含任何规则排列或顺序的固体是非晶态固体。非晶态固体是假固体,而晶体固体是真固体。玻璃是非晶态固体的例子。而金刚石是晶体固体的例子。
常见问题
1. 给出一个离子晶体的例子?
由于离子晶体包含离子键。离子晶体的例子有氯化钠、氟化钠、氯化钾等。
2. 金刚石是离子晶体吗?
金刚石是碳的一种同素异形体,其中碳原子以共价键的形式排列成四面体,因此它是共价晶体,而不是离子晶体。
3. 石英是离子晶体吗?
石英也是一种共价晶体,其中原子通过共价键结合在一起。
4. 非晶态固体加热时会软化吗?
非晶态固体在一定温度范围内加热时会软化。这是因为它们上存在的更强的吸引力在加热时会被破坏。
5. 为什么非晶态固体没有长程有序?
非晶态固体是由快速冷却形成的。因此,它们内部没有足够的粒子。它们只与最近的粒子连接。因此,它们具有短程有序。


 数据结构
数据结构 网络
网络 关系数据库管理系统(RDBMS)
关系数据库管理系统(RDBMS) 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C语言编程
C语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP