氢气
简介
氢原子的重量最轻。氢是一种化学式为𝐻2的常见气体。它由双原子分子组成。除了极易燃烧外,它还无色无味。氢是宇宙中最丰富的化学元素,约占所有普通物质的75%。等离子体氢构成了像太阳这样的恒星的大部分物质。在地球上,氢主要以水分子的形式和有机分子中存在。氢是一种化学元素,原子序数为1,符号为𝐻。氢气的分子式为𝐻2
什么是氢气?
两个氢原子结合形成称为氢气的同核双原子分子。该分子通过它们之间的共价键满足了两个氢原子的可能电子构型。由于氢是目前元素周期表中最轻的元素,因此氢气是最轻的已知分子。氢气是一种无色、无味、无臭的气体,在常温常压条件下极易燃烧。
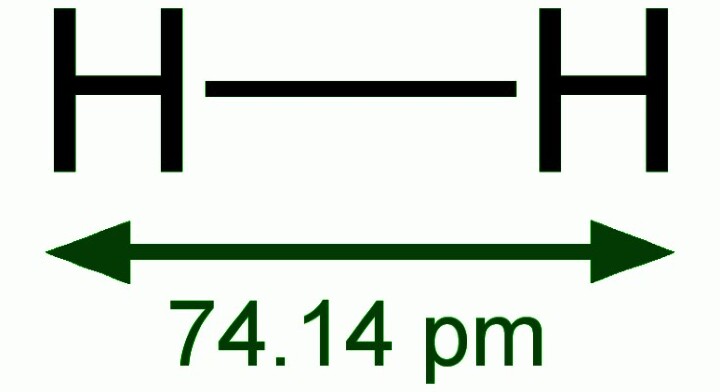
氢气的结构
两个氢原子通过一个共价键结合形成氢气分子。这种分子呈线性结构且是非极性的。每个氢原子都贡献一个电子到共价键中。因此,氢气分子中的两个氢原子可以形成二重态。
氢气的性质
化学性质
氢气是一种非金属。
氢原子用字母“𝐻”表示。然而,它在自然界中以其双原子形式“$\mathrm{H_{2}}$”即氢气出现。
它的性质大多不活泼。氢气是一种稳定的分子,不具有很强的反应活性。
在与金属的反应中,它充当氧化剂。生成金属氢化物。
氢呈中性,因为它不影响石蕊试纸。
氢气具有很高的焓,这归因于强烈的H-H键。
与不饱和烃(如乙烯)反应生成饱和烃。
物理性质
它是我们元素周期表中最轻的元素。分子量为1.00784u。
这种氢双原子分子在室温下以气体形式存在。
它也是所有元素中密度最小的。
它完全无味、无臭、无色,因此非常难以检测。
该气体完全无味、无臭、无色,因此非常难以检测。
它也极易燃烧或易燃。
燃烧时会产生水。燃烧时火焰呈蓝色。它在大约-250℃的温度下液化。
氢气的应用
它被用作液氢火箭燃料。
它用于哈伯法制备氨。
它用作还原剂。
它用于生产合成汽油。
它用于制备金属氢化物。
它用于氢化植物油。
它用于重金属冶金操作。
它在空间研究中用作火箭燃料。
它用于生产$\mathrm{HCl}$。反应如下所示
它用于燃料电池中发电。
它是甲醇生产的一部分
$$\mathrm{Cl_{2}\:+\:H_{2}\:\rightarrow\:2HCl}$$
$$\mathrm{ZnO.CrO_{3}\:+\:H_{2}\:+\:CO\:+\:H_{2}\:\rightarrow\:CH_{3}OH}$$
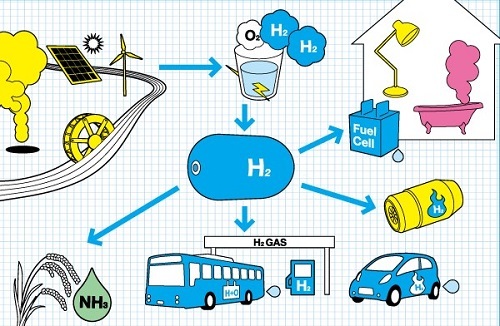
氢气的制备
工业制备
由于在肥料和炼油过程中对氢的需求量巨大,因此氢气的工业生产是一个庞大的产业。
莱恩法
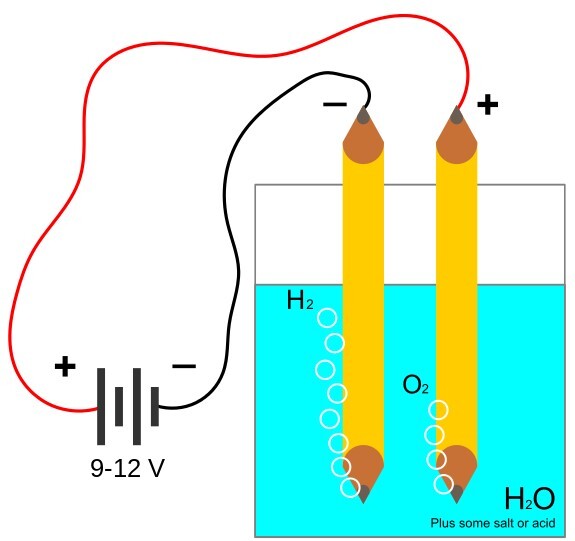
水的电解
在此过程中,水煤气(CO和氢的混合物)和蒸汽交替地在高达8000的温度下通过铁。最初氧化铁会释放氢,然后必须更换铁。然后通过水煤气还原使铁恢复成金属。这些是反应
$$\mathrm{3Fe\:4H_{2}O\:\rightarrow\:Fe_{3}O_{4}\:+\:4H_{2}}$$
$$\mathrm{Fe_{3}O_{4}\:+\:4CO\:\rightarrow\:3Fe\:+\:4CO_{2}}$$
净反应为
$$\mathrm{CO\:+\:H_{2}O\:\rightarrow7bsol;:CO_{2}\:+\:H_{2}}$$
该方法有助于以非常纯净的形式从水中制备氢。当电流通过液体时,水分子被分解。氢气在阴极收集,而氧气在阳极收集。
从天然气中制备
这仍然是目前大规模生产氢气最经济的方法。将气体在高温(高达1100℃)下与蒸汽和𝑁𝑖催化剂一起加热。这导致甲烷分子分解成𝐶𝑂和氢气。
实验室制备
锌与碱的反应
酸与锌的反应
锌也可以与碱性水溶液(如氧化钠)反应,副产物是氢气。反应如下所示。
$$\mathrm{Zn\:+\:2NaOH\:\rightarrow\:Na_{2}ZnO_{2}\:+\:H_{2}}$$
在实验室中,可以通过多种方法使𝑍𝑛与稀酸反应来制备氢气。锌变成硫酸锌(或𝑍𝑛𝑐𝑙2),并释放出氢气。
$$\mathrm{Zn\:+\:H_{2}SO_{4}\:\rightarrow\:ZnSO_{4}\:+\:H_{2}}$$
氢气的生物化学
氢气通常是由于无氧代谢而产生的。它也是许多细菌产生的,通常是通过酶辅助的化学过程。已知称为氢化酶的酶含有铁或镍,并已知催化涉及氢气释放的生物过程。
与氢气相关的危害
几乎所有充当氧化剂或具有一定氧化能力的元素都会与氢气发生反应。即使在低至室温的反应温度下,𝐻2也可以与卤素(如氟和氯)以非常自发和剧烈的方式反应。这些剧烈反应产生卤化氢,包括氯化氢和氟化氢,它们都是潜在的有害酸。
结论
两个氢原子结合形成称为氢气的同核双原子分子。该分子通过它们之间的共价键满足了两个氢原子的必要二重态构型。氢气是有史以来发现的最轻的分子,而氢是现代元素周期表中最轻的元素。氢气是一种无色、无味、无臭的气体,在常温常压条件下极易燃烧。等离子体氢构成了像太阳这样的恒星的大部分物质。在地球上,氢主要以水分子的形式和有机分子中存在。
常见问题
1. 氢气的两种形式是什么?
氢分子可以以邻氢和对氢的形式存在,并且两个原子的核都在自旋。如果原子核的自旋平行且指向同一方向,则该分子被称为邻氢。
2. 氢气分子的形状是什么?
氢气分子是非极性的,呈线性结构。
3. 邻氢和对氢的区别是什么?
邻氢和对氢的原子核具有不同的自旋。邻氢分子的两个原子核都朝同一方向自旋,而对氢分子的两个原子核都朝相反方向自旋。它们具有不同的化学性质,但具有相似的物理性质。
4. 为什么氢气是一种可燃物质?
氢具有非常高的产热量和热值。它的高热值提供了更高的燃烧温度和更长的火焰持续时间。由于氢气的广泛可用性,它可以作为一种经济的商业燃料。
5. 氢气具有哪种类型的键?
两个氢原子通过一个共价键结合形成氢气分子。


 数据结构
数据结构 网络
网络 关系型数据库管理系统
关系型数据库管理系统 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 编程
C 编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP