硅是金属吗
简介
硅是一种具有蓝灰色金属光泽的晶体结构,坚硬而易碎。在元素周期表中,它属于第 14 族;碳位于其上方,锗、锡、铅和钫位于其下方。尽管硅是地球上按质量计算第八丰富的元素,但它很少以纯元素的形式出现在地壳中。工业上使用的硅大部分未分离,天然矿物通常经过非常轻微的加工。

什么是硅?
硅是一种化学元素,原子序数为 14,符号为 Si。硅是七种被称为**准金属**的元素之一。这仅仅是描述一些物质的一种创造性方法,这些物质**不完全**像**金属或非金属**那样运作。它具有四价,是一种准金属,也是一种半导体,具有**蓝灰色**的金属光泽,是**粗糙、晶体和易碎的固体**。
自然界中的存在
硅在地球**地壳中的含量为 27.2%。**
由于**硅酸盐矿物**构成了地球地壳的**90% 以上**,因此硅是继氧之后地壳中**第二丰富的元素**。
自然元素硅在世界海洋中似乎具有**400 年的停留时间**,前提是它尚未存在于那里。
**地球总质量的 68.1%** 由地幔构成,地幔主要由密度更大的**硅酸盐和氧化物**构成,例如(Mg,Fe)2 SiO4,称为**橄榄石**。
大陆岩石的化学风化、河流迁移、陆源碎屑硅酸盐的溶解以及海底玄武岩与热液的反应(释放出结合的硅)是硅通量进一步进入海洋的四个主要贡献者。
硅的性质
硅的物理性质
硅原子有**14 个电子**。
硅是一种明亮的**半导体**,在标准压力和温度下具有蓝灰色的金属光泽,与半导体常见的情况一样,其电阻随着温度升高而降低。
电子与否一样可能存在的能量称为**费米能级**。因此,在环境温度下,纯硅基本上充当**绝缘体**。
在正常情况下,**硅结晶**成巨大的**共价结构,特别是金刚石立方晶格**。
硅的化学性质
硅的 14 个电子在初始状态下排列在电子构型**[Ne]3s2 3p2 中。**
它可以通过产生**sp3 杂化**轨道来耗尽其八隅体并达到氩的理想惰性气体构型,它包含与价轨道相同的价电子数。
硅具有很高的**熔点 1414 °C。**
硅的**沸点约为 3265 °C。**
硅的汽化能力低于碳,这表明**Si-Si 键比 C-C 键弱。**
天然产生的硅的三个稳定同位素是永久同位素28Si、29Si 和30Si。其中只有29Si 可用于 EPR 和 NMR 光谱研究。
硅的化合物/聚合物(硅材料)
已知硅有多种化合物。其中一些在下面讨论 -
硅化物
许多金属硅化物具有从**金属键到离子键到共价键**的键。M5 Si、M6 Si、M15 Si4、M3 Si、M5 Si2、M5 Si3、MSi、M2 Si3、MSi2 等是已知硅化物化学计量的例子。
硅烷
硅烷构成了硅氢化物的同系物序列,其**通式为 Sin H2n+2**。它们都是强还原剂。除了环状 Si5 H10 和 Si6 H12 之外,还已知**高达 n=8** 的长链和支链。
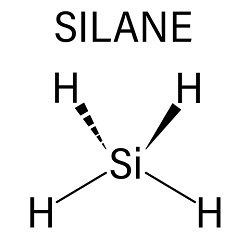
硅烷的最简单形式。
卤化物
所有四个稳定的卤素都可以轻松地与**硅和碳化硅**结合,形成无色、不稳定和易爆的四卤化硅。**卤代聚硅烷** Sin X2n+2类似于硅烷,并且同样众所周知。卤代聚硅烷已发现,至少达到 Si6 Cl14、Si14 F30 和 Si4 Br10。
二氧化硅
仅次于水的研究量是二氧化硅,有时也称为**二氧化硅**(SiO2)。二氧化硅共有 12 种已知的晶体变体,其中**石英**最为常见。大多数二氧化硅的晶体结构由无限的 SiO4 四面体组成。
二氧化硅结构。
有机硅化合物
有机硅化合物通常表现出显着的热稳定性和化学稳定性,这是由于**Si-C 键的强度接近于 C-C 键**。例如,**四苯基硅烷**,即 SiPh4。
硅树脂
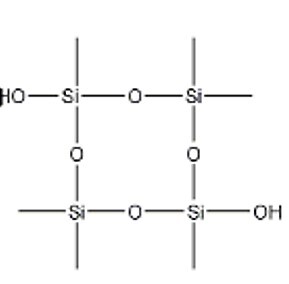
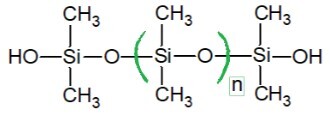
与矿物硅酸盐相比,**硅酮**可以被视为类似物,因为它们的甲基与硅酸盐的**等电子**(O-)部分相匹配。它们提供重要的**防粘、消泡特性和介电特性**,并且对高温、氧化和水具有很强的抵抗力。
硅的用途
许多硅化合物,包括**硅砂、粘土和大多数建筑石材**,都具有直接的商业应用。
硅主要用于**结构化合物**,以二氧化硅、硅酸盐或矿物形式。
**硅片**由单晶硅制成,用于电子、半导体行业。
**耐火砖**,一种陶瓷,由二氧化硅制成。**白瓷陶瓷**也包括硅酸盐矿物。
有趣的事实
尽管有些人可能认为,**硅和硅酮**完全不同。硅酮是一种由硅氧聚合物组成的**人工物质**。**硅是一种天然存在的元素。**
**纯硅**的晶格与**金刚石**(由碳构成,碳是硅在第 14 族中的上方元素)的晶格相同。
结论
硅主要以不同类型的**二氧化硅或硅酸盐的形式广泛分布在宇宙尘埃、小行星和行星**的空间中。按质量计算,硅是宇宙中**第八丰富的元素**,但它很少以纯元素的形式出现在地壳中。在**技术和电子行业**,硅是最重要的半导体。
常见问题
1. 为什么硅被称为硅?
硅的名称源于拉丁语**silex**,通常称为 silicis,意为**“坚硬的石头”或“燧石”**。
2. 硅金属有毒吗?
以元素或其任何原始形式(包括二氧化硅和硅酸盐)存在时,这些都是最普遍的,**硅无毒。**
3. 你可以在人体中找到硅吗?
大多数**生物组织、骨骼组织和软组织**都含有大量的硅。
4. 硅可以形成有限数量的键吗?
是的,与碳一样,硅是四价的。因此,它可以轻松地与某些其他原子共享其所有四个轨道电子,从而与它们形成共价键。
5. 硅可以同时形成多个键吗?
由于 p-d 键重叠不足,硅**无法形成 Si=Si**。由于其尺寸,Si 几乎没有倾向于与自身形成双键。


 数据结构
数据结构 网络
网络 关系数据库管理系统
关系数据库管理系统 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 语言编程
C 语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP