钾
介绍
钾元素最早由著名的英国化学家汉弗里·戴维爵士于1807年发现。该元素最初是从熔融态的苛性钾(KOH)化合物中通过电解分离出来的。然而,钾是在电解系统中的阴极收集到的。

图1:钾:化学元素特性及用途
钾及其存在形式
钾被认为是第二轻的元素,简单来说,钾的密度仅次于锂。钾的符号为K,来源于拉丁语Kalium。这种化学元素属于碱金属。人们注意到,钾在室温或常温下呈固态。
钾是一种柔软的金属,呈银白色,其同位素在地球上广泛存在。钾主要存在于火成岩、页岩以及包括正长石和白云母在内的各种矿物沉积物中。然而,收集钾元素相当困难,因为与钾相关的元素完全不溶于水。
溶于水的钾化合物包括光卤石(KMgCl₃·6H₂O)、泻利盐(K₂Mg₂[SO₄]₃)、多卤石(K₂Ca₂Mg[SO₄]₄·2H₂O)以及钾盐(KCl)。然而,这些元素存在于古老的河床和海底之下。这些元素经过电解后用于商业用途。
钾作为一种金属
钾金属被认为是地球上最丰富的元素之一,排名第七。根据记录,地球地壳约有2.4%是由这种元素构成的。
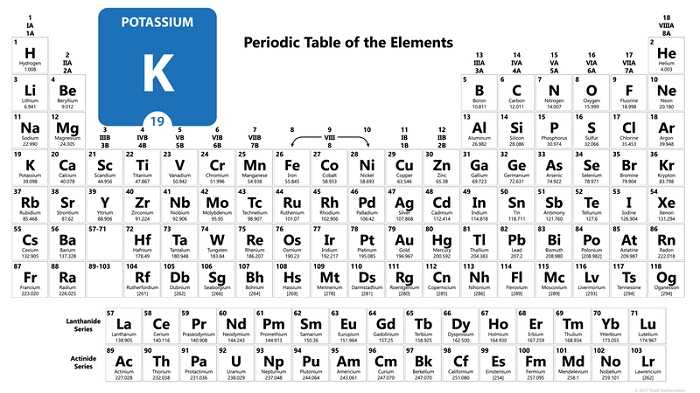
图2:元素周期表中的钾
钾的沉积物以氯化钾化合物的形式存在,数量超过十亿吨。这种元素在动植物的生命中不可或缺。该元素的原子序数为19,原子质量为39.0983 amu(原子质量单位)。
同位素
钾元素有三种重要的同位素,包括39、40和41。其中,钾-40具有高度反应活性,存在于岩石、动物和植物中。
同位素主要用于测量物体的年龄。然而,当存在氩同位素时,同位素会发生衰变。
物理和化学性质
钾元素的熔点和沸点分别为63℃和770℃。就其物理性质而言,钾漂浮在水上,分离后的元素具有延展性,呈银白色。就化学特性而言,钾与水剧烈反应生成氢气,因此很容易着火并爆炸。这种元素很容易与磷、氯、硫、氮反应,其蒸汽呈绿色,火焰呈淡紫色。
反应
钾与水剧烈反应,释放出氢气,反应速度很快。反应式为:
$\mathrm{“2K(s) + 2H_2O\:\rightarrow\:2KOH (aq) + H_2 (g)”.}$
在空气中,钾会变成暗淡的颜色,反应式为:
$\mathrm{“K(s) + O_2(g)\:\rightarrow\:KO_2(s)”.}$
钾:应用和一般事实
钾的应用多种多样,包括用作注射剂的氯化钾,用于制造肥皂和洗涤剂的钾碱。此外,钾还用于核电站的热交换器,钾盐用于肥料。
电解过程中最关键的事实是钾是第一种被分离出来的金属。这是因为在此之前,很难区分钠和钾元素。在被识别之前,钾已被用于与动物脂肪混合生产肥皂,以及生产碳酸钾。
结论
在本教程中,我们重点关注了钾元素。人们注意到,钾是地球上最丰富的元素之一,约占地壳的2.4%。然而,它以化合物的形式存在,并通过电解过程分离出来。
(常见问题)
Q1. 为什么钾元素在化学领域很重要?
A1. 钾元素在化学领域至关重要,因为它在维持活细胞的正常功能方面起着关键作用。它也用于神经功能并维持人体内的整个液体系统。
Q2. 钾的五个最重要的工业用途是什么?
A2. 钾金属由于其广泛的应用而对工业用途有利。钾用于制造用于卫生目的的肥皂和洗涤剂。在黄金开采中使用钾,它还用于生产玻璃和染料。此外,它还用于制造电池和火药。
Q3. 钾元素的另一个名称是什么?
A3. 钾元素的另一个名称是钾碱,取自英文单词,但其化学符号取自拉丁语Kalium。Kalium 一词是中古拉丁语中钾碱的词,源于阿拉伯语qali,意思是碱。


 数据结构
数据结构 网络
网络 关系数据库管理系统 (RDBMS)
关系数据库管理系统 (RDBMS) 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C语言编程
C语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP