三氟化氯
介绍
三氟化氯 (ClF3) 具有高度的可燃性和爆炸性。在第二次世界大战期间,纳粹对 ClF3 感兴趣,试图将其用于制造强大的炸弹。然而,由于其易挥发和反应性强烈的特性,其生产被减少了。这就是为什么战后它从未被用于战斗的主要原因。由于其破坏性,三氟化氯在《化学武器公约》中被禁止,其生产量甚至限制在 30 吨以内。
什么是三氟化氯?
在 20 世纪 30 年代,两位科学家奥托·鲁夫 (Otto Ruff) 和 H. 克鲁格 (H. Krug) 发现了一种比氟更具反应性的液态化合物,他们分离出了三氟化氯 (ClF3)。它可以定义为一种由化学式 ClF3 表示的互卤化物化合物。它也称为氯氟化物和三氟-λ3-氯烷。这种气体如果有人靠近会造成肺损伤。除此之外,它还会刺激皮肤、眼睛和粘膜。ClF3 被认为是最强的氧化剂之一,它与任何易燃物质接触都会着火。
三氟化氯的结构

图 1 - 三氟化氯
三氟化氯,公共领域,来自维基共享资源
就分子几何而言,ClF3 具有两个长键和一个短键,由于这些键,它呈现T字型形状。在 ClF3 分子中,氯原子位于中心。它有五个区域电子密度:三个键和两个孤对电子。ClF3 的结构遵循 VSEPR 理论,因为存在于两个赤道位置的孤对电子呈三角双锥形排列。它们的 F-Cl-F 键角为 175 度。由于超价键合,Cl-F 键是稳定的。在石英容器中,ClF3 在 180°C 以下被认为是稳定的,高于此温度,它会分解成其组成元素,这是由于自由基机制造成的。
三氟化氯的性质
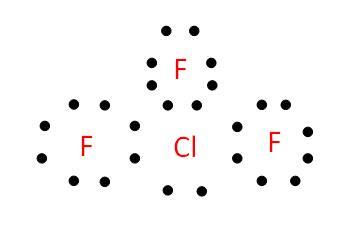
图 2 - 三氟化氯的电子结构
ClF3 是一种在自然界中找不到游离状态的化合物。作为一种化合物,它不仅危险,而且高度易燃。它的密度为 **1.77g/cm3**,摩尔质量为 **92.448g/mol**。ClF3 的沸点和熔点分别为 **11.75°C** 和 **-76.34°C**。在 ClF3 的结构中,存在 4 个原子,它也具有一个共价键合单元,此外,它可以溶于水。气态或蒸汽状态的 ClF3 可以分解成 ClF、ClOF、ClO2F、ClO3F、Cl2 和 HF。最后三个是最重要的。然而,结果总是取决于水的可用性。
三氟化氯的制备
ClF3 可以通过氯气和氟气直接反应制备。该反应可表示为:
$$ \mathrm{Cl_{2}\:+\:3F_{2}\:\rightarrow\:2ClF_{3}} $$
另一方面,它可以通过 ClF 和氯气之间的反应制备。它可以用方程式表示,即:
$$ \mathrm{ClF\:+\:F_{2}\:\rightarrow\:ClF_{3}} $$
三氟化氯的用途
ClF3 可用作氟化剂。
它可用作火箭的点火剂和推进剂。
ClF3 被认为是制造核燃料的最重要组成部分。
它在氟碳聚合物的热解抑制剂中起着重要作用。
它用于将铀转化为气态六氟化铀。
它用于清洁半导体工业中的化学气相沉积。
ClF3 与磷反应生成 PCl3(三氯化磷)和 PF5(五氟化磷)。
关于三氟化氯的事实
ClF3 有许多重要的方面。如果 ClF3 与任何元素接触,它会经历蒸发过程并转化为有毒气体。对于实验室实验,如果 400 ppm 的 ClF3 暴露 30 分钟,会造成老鼠死亡。除此之外,ClF3 共有 28 个价电子,键存在于 Cl 原子与其周围的氟原子之间。此外,在分解过程中,ClF3 会产生以蒸汽形式存在的氢氟酸和盐酸。
结论
ClF3 是最危险的化合物之一,由于其易燃性而被认为是危险的。它甚至可以点燃一些最不易燃的物质,例如沙子、玻璃甚至石棉。最危险的部分是它可以与燃烧后的元素如灰烬发生燃烧反应。然而,由于其多用途,它仍然被认为是有用的。
常见问题
1. 三氟化氯的主要用途是什么?
三氟化氯的主要用途是作为火箭燃料,也可用于核反应堆燃料的加工。
2. 三氟化氯易燃的根本原因是什么?
三氟化氯易燃的原因在于其氧化性。它的氧化性比氧气本身更强。它不仅易燃,而且由于其氧化性而被认为是一种极其有效的爆炸物。
3. 三氟化氯的常用名称是什么?
三氟化氯也称为氯氟化物,表示为 ClF3。
4. 三氟化氯是如何形成的?
三氟化氯是由中间的氯阳离子和与之结合的三个氟阴离子形成的。
5. 三氟化氯的颜色是什么?
三氟化氯的气态形式呈无色,而液态形式呈绿色,并具有刺鼻的气味。


 数据结构
数据结构 网络
网络 关系数据库管理系统 (RDBMS)
关系数据库管理系统 (RDBMS) 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C语言编程
C语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP