电子和质子的区别
根据**物质电子理论**,所有物质都是由称为分子的微小粒子组成的。而分子又是由**原子**组成的。因此,原子是物质的基本组成部分。
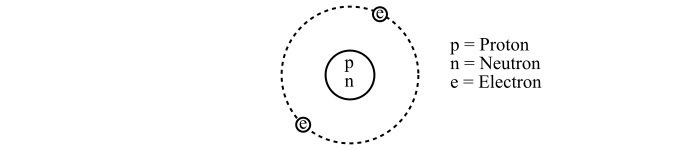
一个原子由两个主要部分组成,即**原子核**和**核外电子**。原子核是原子的中心部分,包含两个亚原子粒子,即**质子**和**中子**。而核外电子则是围绕原子核在不同轨道上运行的电子的空间。
在本文中,我们将列出电子和质子之间所有主要的区别。尽管电子和质子都是亚原子粒子,但它们也被称为电粒子,因为它们充当物质中的电荷载体。
什么是电子?
**电子**是一种亚原子粒子,带负电荷。在原子内部,电子存在于原子的核外,并在轨道上围绕原子核运动。
电子用符号“e”表示。电子携带的负电荷等于-1.6 × 10-19 C。电子的质量为9.1 × 10-31 kg。英国物理学家**J. J. 汤姆逊**于1897年发现了电子。电子是解释科学中多种现象(如电、磁、化学键合、热传导等)的关键粒子。
什么是质子?
**质子**是一种亚原子粒子,带正电荷。质子位于原子核内,使原子核带正电。
质子通常用符号“p”表示。质子的发现归功于**欧内斯特·卢瑟福**,他在1917年提出每个原子在其原子核中都存在一个带正电的粒子。质子携带的电荷量等于电子的电荷量,即+1.6 × 10-19 C,而质子的质量等于1.67 × 10-27 kg。
电子和质子的区别
质子和电子都是原子的亚原子粒子,分别带正电和负电。然而,质子和电子之间存在许多差异,在下表中进行了重点说明:
差异依据 | 电子 | 质子 |
|---|---|---|
定义 | 电子是一种带负电的亚原子粒子。 | 质子是一种带正电的亚原子粒子。 |
表示方式 | 电子通常用符号“e”表示。 | 质子通常用符号“p”表示。 |
电荷极性 | 电子携带负电荷。 | 质子携带正电荷。 |
电荷值 | 一个电子的电荷等于-1.6 × 10-19 C。 | 一个质子的电荷等于+1.6 × 10-19 C。 |
质量 | 电子的质量小于质子,等于9.1 × 10-31 kg。 | 质子的质量大于电子,等于1.67 × 10-27 kg。 |
原子内部位置 | 电子存在于原子核周围的空间,称为核外电子。 | 质子存在于原子核内。 |
迁移性 | 电子可以在原子核周围的特定轨道上自由移动。 | 质子不具有迁移性,因为它们位于原子核内,并受到核力的强烈束缚。 |
添加或移除 | 电子可以轻松地添加到或从原子中移除。 | 在原子中添加或移除质子非常困难。 |
参与反应 | 电子参与化学反应。 | 质子通常不参与正常的化学反应,但它们可以参与核反应。 |
参与电流流动 | 电子完全负责电流的流动。 | 质子不参与电流的流动。 |
结论
电子和质子都是原子中的亚原子粒子。上表列出了电子和质子之间所有主要的区别。最显著的区别在于电子是带负电的粒子,存在于原子核周围的轨道上,而质子是带正电的粒子,存在于原子核内。

广告

 数据结构
数据结构 网络
网络 关系型数据库管理系统 (RDBMS)
关系型数据库管理系统 (RDBMS) 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 编程
C 编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP