分子与化合物之间的区别
简介
分子和化合物之间存在着重大的区别,每个人都应该了解。当化学键连接任意两个或多个原子时,就会形成分子。而化合物是由不同化学元素的不同原子组成的分子。所有化合物都是分子,但并非所有分子都是化合物。分子仅仅是任何原子的组合。但是,当原子组合不同于元素时,就被称为化合物。氢气 (H2) 和氧气 (O2) 都是分子,因为它们包含两个或多个原子。而碳酸钙 (CaCO3)、NaCl 和 H2O 被归类为化合物,因为它们包含不同的成分。
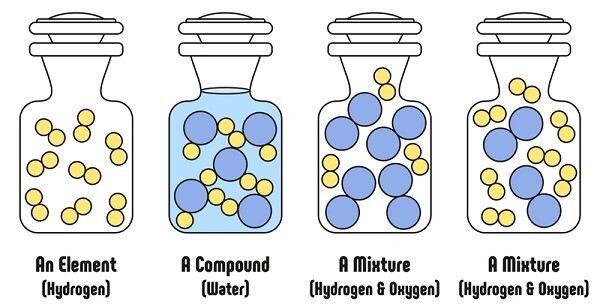
什么是分子?
它是构成化学元素的成分的最小粒子,其特性与元素的特性基本相同。它们由通过重要的化学键结合在一起的原子组成。这种键可能是电价键,即通过共享电子形成,也可能是共价键,即通过交换电子形成。它们与离子的区别在于它们的性质是中性的,这意味着它们既没有正 (+) 电荷,也没有负 (-) 电荷。它们仅仅由 2 个原子的反应产生。例如,N2、O2 和 H2。
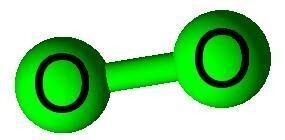
同核与异核
| 同核双原子分子 | 异核双原子分子 |
|---|---|
| 它们由两个通过共价键结合在一起的相同化学元素的原子组成。 | 它们是由两个不同化学元素的两个原子通过共价键结合在一起形成的化合物。 |
| 稳定同位素非常稳定,但不会发生放射性衰变。 | 它们具有不同化学元素的原子。 |
| 它们具有非极性共价键。 | 它们具有极性共价键。 |
| 它们具有相同的原子。 | 它们具有不同的原子。 |
化合物的定义
它们是由来自不同元素的原子的化学键合产生的化学化合物。这些不同的原子各自具有不同的电荷;带正 (+) 电荷的(原子)是电子亏损的,而带负 (-) 电荷的(原子)是电子富裕的。通过结合在一起从而生成新的分子,这两个不同的原子结合在一起以达到中性。例如,带正电荷的氢原子 H+ 和带负电荷的氧 (O) 原子以比例质量化学结合形成水 (H2O)。因此,水是一种化合物,因为它是由两种不同的元素,氢和氧的结合产生的。二氧化碳也是化合物的一个例子。
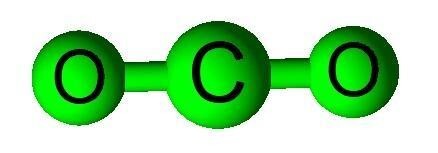
化学式
它们以它们的化学式来区分。化学式详细说明了构成特定化学化合物的原子碎片。水的化学式为 H2O,表示两个氢原子和一个氧原子结合形成一个 H2O。食盐的化学式为氯化钠 (NaCl),这表明一个钠 (Na) 原子和一个氯 (Cl) 原子结合形成一个氯化钠 (NaCl)。
化合物的类型
根据它们的来源,它们被分为两类。
无机化合物 - 它们通常从非生物来源(如岩石和矿物)中获得。例如,食盐、大理石、苏打、小苏打、二氧化碳、氨、硫酸等
有机化合物 - “有机”一词指的是生物体中发现的各种器官。有机化合物是由活生物体(如植物和动物)形成的。碳 (C) 已被确定为所有有机分子中的重要组成部分。它们通常被称为碳 (C) 化合物。例如,甲烷、乙烷、丙烷、酒精、醋酸、糖、蛋白质、油脂、脂类等
根据它们的特性,它们被分为三类。
酸 是酸性的化学化合物,它们与水 (H2O) 反应,使蓝色石蕊试纸变红。例如,硫酸 (H2SO4)、乳酸 (C3H6O3)、盐酸 (HCl)、柠檬酸 (C6H6O7)、碳酸 (H2CO3)、硝酸 (HNO3) 等。
碱 是苦味的化学化合物,它们与水 (H2O) 反应,使红色石蕊试纸变蓝。例如,氢氧化钙 Ca(OH)2、氢氧化镁 Mg(OH)2、氢氧化钠 (NaOH) 等。
盐 由酸和碱的相互作用形成。例如,氯化钠 (NaCl)、氯化钙 (CaCl2)、硝酸钙、硫酸锌等。
化合物的例子
NaCl(盐)
H2O2(过氧化氢)
C2H6O(酒精)
CH4(甲烷)
C55H72O5N4Mg(叶绿素)
一些常用化合物的例子及其分子式
| 俗名 | 化学化合物 | 化学式 |
|---|---|---|
| 泻盐 | 七水硫酸镁 | MgSO4·7H2O |
| 漂白水/次氯酸钠 | 次氯酸钠 | NaOCl/NaClO |
| 漂白粉 | 氯氧化钙 | CaOCl2 |
| 干冰 | 固体二氧化碳 | CO2 |
| 苛性钾 | 氢氧化钾 | KOH |
| 氯仿 | 三氯甲烷 | CHCl3 |
| 酒石酸氢钾 | 酒石酸氢钾/酒石酸钾 | KC4H5O6 |
| 白云石 | 碳酸钙镁 | CaMg(CO3)2 |
| 甘汞 | 氯化亚汞 | Hg2Cl2 |
| 硼砂 | 十水四硼酸钠/硼酸钠 | Na2B4O7·10H2O |
| 芒硝 | 十水硫酸钠 | Na2SO4·10H2O |
| 甘油 | 丙三醇 | C3H8O3 |
| 石膏 | 二水硫酸钙 | CaSO4·2H2O |
| 小苏打 | 碳酸氢钠或碳酸氢钠 | NaHCO3 |
分子和化合物的区别
| 分子 | 化合物 |
|---|---|
| 它们由两个或多个通过化学键连接的原子组成。 | 它们由两个或多个通过化学键结合的不同元素组成。 |
| 它们可能是异核的,也可能是同核的。 | 它们由多种成分组成。 |
| 可能易挥发。 | 由于它们处于物理形态,因此它们始终稳定。 |
| 共价键或离子键 | 离子键、金属键或共价键 |
| 并非所有分子都是化合物。 | 所有化合物都是分子。 |
| 肉眼不可见 | 肉眼易见 |
| 一组通过强大的力量结合在一起的原子 | 整体的真实物质 |
结论
因此,很明显分子和化合物是如何相关的,尽管两者都具有不同的特征,包括基于其成分以及原子的特征。每个分子的质量根据其形成的原子而有所不同,因此每个化合物的质量也不同。除了质量之外,其他性质如硬度、颜色、状态等都依赖于原子,因为原子是分子和化合物都依赖的基本单位。水、甲烷以及温室气体都是既是分子又是化合物的例子。
常见问题
1. 分子的不同种类有哪些?
单原子分子是指仅包含一个元素的原子的分子。例如,Na、He 等。双原子分子是指在一个元素的分子中具有两个原子的分子。例如,O2 和 N2。多原子分子是指在一个元素的分子中具有两个以上原子的分子。例如,P4、S8 等。
2. 分享一些分子的实例。
臭氧、氧分子和氮都是分子的例子。
3. 根据其键,化合物的 3 种类型是什么?
离子化合物、共价化合物和配位化合物是 3 种类型的化合物。
4. 分子是否可以只有一个原子?
它被定义为通过化学键结合在一起的两个或多个原子的电中性集合。因此,根据定义,分子不能由单个原子产生。
5. 当原子结合形成分子时,会发生什么?
当原子结合形成分子时,化学键将它们结合在一起。这些键是在原子共享或交换电子时形成的。只有最外层壳层的电子具有结合活性。


 数据结构
数据结构 网络
网络 关系型数据库管理系统
关系型数据库管理系统 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 语言编程
C 语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP