电极
简介
电极这个名称是由科学家威廉·惠威尔首次提出的。它源于希腊词“Elektron”和“hodos”,分别意为“琥珀”和“道路”。电极具有高度导电性,因此在许多领域都有应用。静电计是电极的早期版本,由科学家约翰·威尔克发现,用于研究静电。它也被用作电流进入或离开系统的术语。自从电极被发现以来,它们就成为电池和电池的重要组成部分。后来,根据用途引入了不同类型的电极。1839年,约翰·弗雷德里克·丹尼尔发现了第一块电池——丹尼尔电池。
什么是电极?
发生氧化反应或电子离开电池的点是阳极。而发生还原反应或电子进入电池的点是阴极。任何金属电极都不能永久地作为阳极或阴极。电极的性质(阴极或阳极)会随着电子流动方向而变化。它将取决于金属的氧化还原电位。还有一种称为双极的电极,它可以同时改变其阴极和阳极的性质。

电化学电池中的阴极和阳极
阳极和阴极是从希腊语派生出的重要术语,在电化学应用中起着重要作用。阳极是负电极,可以在电化学回路中释放电子。因此,该电极在过程中发生氧化反应。电子通过该电极进入特定系统。而阴极是正电极,可以在电化学回路中接受电子。因此,它是电极在过程中发生还原反应。电子通过该电极离开特定系统。
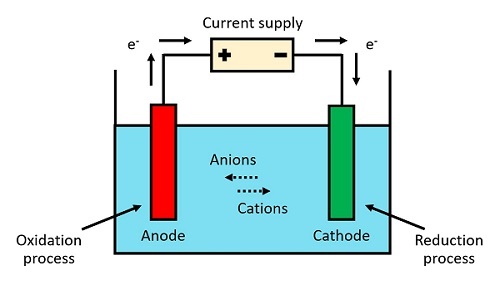
Emanuele Oddo,电氧化装置,CC BY-SA 4.0
下面列出了与阴极和阳极相关的一些要点。
| 阳极 | 阴极 |
|---|---|
| 电子给予体。 | 电子受体。 |
| 负电极。 | 正电极。 |
| 发生氧化反应。 | 发生还原反应。 |
| 电流将通过此进入。 | 电流将由此离开。 |
电极的类型
根据电流进入的方式,电极分为两种类型:正电极和负电极。根据电极的性质,电极通常分为五种不同的类型。
金属-金属离子电极 - 这种类型的电极中,金属电极依赖于含有与金属相同离子的溶液或电解质。这种电极中的阴极是氧化电位较低的电极,它会发生还原反应。而这种电极中的阳极是氧化电位较高的电极,因此它会发生氧化反应。这种电极中的电流交换发生在金属电极和电解质中金属离子之间。例如,铜电极浸入硫酸铜溶液中。
金属-不溶性盐电极 - 在这种电极中,不溶性盐涂覆在金属电极上。然后将涂覆的电极浸入含有盐阴离子的溶液中。并且可逆于不溶性盐中存在的阴离子。甘汞电极是此类别的示例。
金属-汞齐电极 - 由于钠和钾等金属的高反应活性,引入了金属汞齐电极。因为通过引入其汞齐形式(即用汞稀释)降低了此类金属的反应活性。这种类型的电子中使用的电解质是金属离子本身的溶液。
气体-离子电极 - 在这种类型的电极中,气体不断地通过含有惰性金属(如铂和金)的溶液鼓泡,该溶液浸入含有气体阴离子或阳离子的溶液中。最常用的气体是氢气,但也使用其他一些气体,如氯气和氧气。这种类型的电极中使用的惰性电极仅有助于保持电接触,它不会在这种电极中发生反应。在气体和离子之间会发生电子转移。例如,标准氢电极。
氧化还原电极 - 在这种类型的电极中,氧化还原反应将会发生。对于这种电极,溶液含有将要浸入两种不同氧化态的金属离子。电极中使用的惰性金属充当电子的来源和电子受体。例如,这种电极包含金属铁的铁离子和亚铁离子。
电极的用途
电极在电化学中非常重要。因此,电极的用途是:
它存在于电化学电池和电池中。并且是电流流动的必要条件。
用于测量 pH 值,使用玻璃电极。
在电解过程中,可以借助电极测量电导率。
它存在于生物化学应用中的生物电学中。
它存在于焊接设备中。
它存在于心电图中。
它们用于燃料电池。
电极用于电镀目的。
它用于阴极保护。
在纳米电化学领域,使用纳米电极。
它用于接地目的。
结论
电极是良好的导体,存在于电化学电池的应用中。它充当非金属材料中的导体。它们主要分为两种类型:负电极和正电极。分类基于电流的流动。阳极和阴极电极始终存在于所有电化学应用中。但是,根据电极的性质及其应用,电极也有一些其他的分类。金属-金属离子电极、氧化还原电极等就是其中一些。电极的用途也很广泛。电极存在于电池、电池、焊接应用、心电图、接地目的、pH 测量等中。
常见问题
1. 什么是克拉克氧电极?
在这种电极中,铂用作阴极,银用作阳极。氧气多孔膜用于将电极与饱和氯化钾溶液分离。
2. 什么是阴极保护?
这是一种提供给易腐蚀金属的保护。其中,金属充当电化学电池的阴极。它使用易腐蚀的牺牲金属或金属作为阳极来保护此阴极。
3. 为什么进行接地?
为了保护房屋和家用电器免受高电压损坏,进行接地。为此过程使用具有高导电性的电极。金属铜最常用于此目的。
4. 什么是离子选择性电极?
离子选择性电极是一种电分析技术,用于测量溶液中存在的离子的活性。这是一种分析技术,但它测量的是活性,而不是测量离子的浓度。它涉及电位的测量。
5. 什么是化学中的甘汞电极?
这是一种参比电极,包含元素汞和氯化汞。它通常存在于 pH计和电压计中。因为它可以测量 pH 值和电压。


 数据结构
数据结构 网络
网络 关系型数据库管理系统
关系型数据库管理系统 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 语言编程
C 语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP