(a) 描述玻尔原子模型。尼尔斯·玻尔是如何解释原子稳定性的?(b) 某元素的原子序数为11,质量数为23。其电子在各电子层上的排布如何?说明该元素原子核的组成。
(a) 玻尔原子模型
原子由三种粒子构成:电子、质子和中子。
- 质子和中子位于原子中心的微小原子核内。
- 电子以高速围绕原子核旋转,沿着固定的圆形轨道运行,这些轨道被称为能级或电子层。
- 每个能级所能容纳的电子数量是有限的。
- 每个能级都与一定的能量相关联。
- 只要电子在同一能级上运行,其能量就不会发生变化,原子保持稳定。
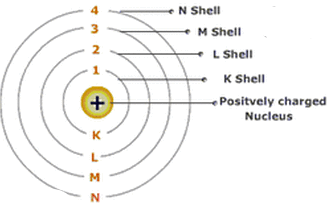
尼尔斯·玻尔通过电子在不同能级上运行的概念解释了原子的稳定性。电子的能量变化发生在它从低能级跃迁到高能级或反之亦然时。
当电子获得能量时,它会从低能级跃迁到高能级;当它失去能量时,它会从高能级跃迁到低能级。这样,能量就不会损失,原子保持稳定。
(b) 原子序数 = 11
质量数 = 23,
电子排布 – (2, 8, 1)
K L M
2 8 1
该元素原子核的组成是11 个质子和 12 个中子。

广告

 数据结构
数据结构 网络
网络 关系型数据库管理系统
关系型数据库管理系统 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 语言编程
C 语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP