化学定律
介绍
化学定律是由几位科学家通过各自的实验确定的。多年来,为了理解我们周围发生的与化学领域相关的自然规律,许多定律被提出、修改和修正。然而,某些定律被认为是化学中最基本的,例如,**质量守恒定律**。其他定律,例如能量守恒定律、查理定律等等,都遵循这一定律。
什么是理想气体和真实气体?
理想气体被定义为完美的气体,它支持建立压力(P)、气体量(n)、温度(T)和体积(V)等变量之间存在的定量关系。然而,这是一种理论上的物质,其特性包括:气体粒子非常小,似乎不占据任何空间;运动是恒定的、随机的以及直线运动。另一方面,真实气体具有相当大的体积,并表现出非弹性碰撞。
玻意耳定律
根据玻意耳定律,气体变量(例如,**体积和压力**)之间存在着重要的关系。然而,在应用此定律时,必须保持气体的**温度和摩尔数**不变。该定律指出,给定质量的理想气体所施加的绝对压力与其在任何封闭系统中的体积成反比。该定律表示为:
$$\mathrm{P\:\varpropto\:\frac{1}{V}\:or\:,\:P\:=\:\frac{x}{V}\:or\:,\:PV\:=\:x\:,\:其中x为常数}$$
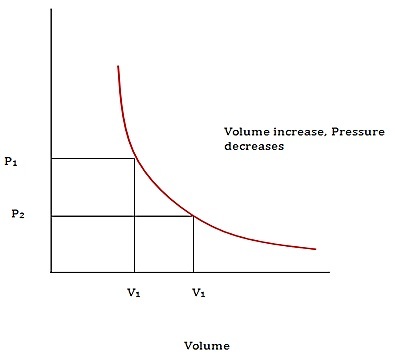
图1 - 玻意耳定律
查理定律
著名的科学家雅克·查理发现了确定气体温度和体积变量之间关系的定律。在此定律中,摩尔数和压力保持不变。该定律指出,气体的体积与其温度成正比。该定律表示为:
$$\mathrm{V\:\varpropto\:T\:or\:,\:V\:=\:yT\:其中y为常数}$$
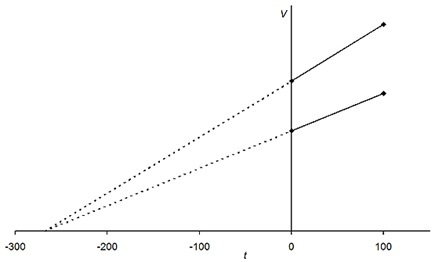
图2:查理定律
阿伏加德罗定律
阿伏加德罗定律主要解决了与盖-吕萨克定律相关的问题。在此定律中,阿伏加德罗指出,在**相同温度和压力**下,不同气体的等体积包含相同数量的分子。该定律的数学表示为:
$$\mathrm{V\varpropto\:n\:or\:,\:V\:=\:zn\:,\:其中z为常数}$$
这里,气体体积之间的关系与其分子数成正比。
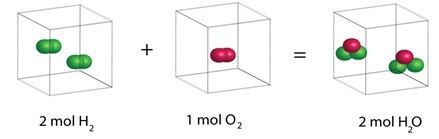
图3 - 阿伏加德罗定律
知识共享署名-相同方式共享4.0,公共领域,来自维基共享资源
理想气体状态方程
理想气体状态方程综合了三个简单的气体定律,并根据气体的体积表示。该定律似乎与所述气体的体积成正比和反比。表示为:
$$\mathrm{V\:\varpropto\:\frac{nT}{P}\:or\:V\:=\:R\frac{nT}{P}\:or\:,\:V\:=\:\frac{nRT}{P}\:or\:,\:PV\:=\:nRT}$$
这里,R是通用气体常数,n表示分子数,P表示理想气体的绝对压力,T表示绝对温度,V表示气体体积。
质量守恒定律
质量守恒定律被认为是化学领域的基本定律,它指出质量既不能被创造也不能被消灭,而只是从一种形式转化为另一种形式。
能量守恒定律
能量守恒定律被定义为一个与周围环境隔离的系统,系统的总能量守恒。
结论
在本教程中,主要关注的是确定化学定律,这些定律倾向于建立自然界同时发生的许多现象。然而,讨论的某些定律如下:能量守恒定律、质量守恒定律表明它们之间存在着复杂的关系。然而,诸如玻意耳定律、查理定律等等定律表明气体变量之间存在着确定的关系。
常见问题解答
1. 热力学定律是什么?
为了定义表征处于热力学平衡点的热力学系统的基本物理量,主要有四个热力学定律被认为是至关重要的。这四个定律分别是:**热力学第零定律、第一定律、第二定律和第三定律**。
2. 法拉第定律是什么?
法拉第定律处理的是导线线圈周围磁场环境的变化,从而导致线圈中产生感应电动势(emf)。然而,需要理解的是,电压的产生并不取决于变化发生的方式。该定律进一步指出,从电极释放的净物质与通过的净电量成正比。
3. 化学领域中最基本的定律是什么?
根据化学领域中所述的定律,质量守恒定律被认为是最基本的定律,因为该定律是关于在任何化学反应中物质的量保持不变。


 数据结构
数据结构 网络
网络 关系数据库管理系统 (RDBMS)
关系数据库管理系统 (RDBMS) 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C语言编程
C语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP