铬
简介
铬是一种硬金属,呈银灰色。铬的电子构型通常表示为$\mathrm{Ar\:3d^{5}\:4s^{1}}$。铬的电子构型主要通过半充满的d轨道来解释,这主要负责提供稳定性。Cr的氧化态为三价,对人类至关重要。这种营养素可以在人体胰岛素、脂类代谢、脂肪酸以及血糖的微量元素中找到。
什么是铬?
铬指的是一种光泽度高、熔点高的金属。通常使用硅热反应和铝热反应从铬铁矿和铬金属中商业化生产铬铁合金。

铬矿石
该反应主要通过焙烧和浸出过程进行。然后,它随后进行碳还原,再进行铝还原。
铬:化学性质
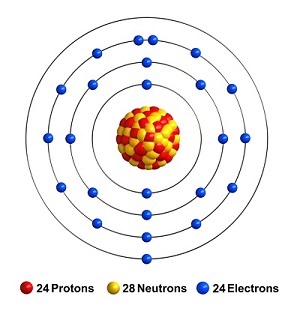
铬的电子构型为$\mathrm{[Ar]3d^{5}\:4S^{1}}$,ChemSpider ID 为 22407,它指的是一个免费的化学结构数据库。这种金属的相对原子质量为51.996 g/mol,铬的关键同位素是52Cr。这种金属的CAS号为7440-47-3。如果加热,这种金属会燃烧,金属化合物会形成绿色的氧化铬。
铬:物理性质
这种金属的原子序数为24,属于第6族。这种金属的周期为第4周期,属于d区元素。铬的元素类别为过渡金属。这种金属的熔点约为2180K或1907°C,沸点约为2944K或2671°C。
铬的密度在20°C时为7.19 g/cm3,熔化热为21.0 kJ/mol。这种金属的汽化热为347 kJ/mol。
铬:应用
在不锈钢行业中,这种金属被广泛应用,对制造和生产各种类型的合金非常有帮助。铬镀层使不锈钢具有镜面效果。例如,汽车的车牌是由这种金属制成的。
铬的主要矿石是铬铁矿,也用于不锈钢部件。
通过使用这种金属,我们可以使一些宝石更加鲜艳。例如,使用铬可以使红宝石更加鲜艳,而祖母绿的绿色则是由铬产生的。
许多汽车装饰包含这种金属或其合金。
电镀是这种金属最重要的应用之一。例如,汽车的亮闪闪的装饰帽是由这种金属制成的。
不锈钢和铝合金是一些重要的合金,在不同的行业中被广泛使用。
铬可以在油漆和染料中看到。一些铬的“化学成分”用于织物。
铬:反应
铬可以在200-300 atm的大气压和400°C的温度下与氟反应。该反应生成六氟化铬,用CrF6表示。反应表示为:
铬还可以与不同类型的酸反应。这种金属的Cr元素主要溶解在稀盐酸溶液中,形成Cr离子以及H气体。它也与硫酸反应,但通常不与硝酸反应。与盐酸的反应表示为:
$$\mathrm{Cr(s)\:+\:3F_{2}(g)\:\rightarrow\:CrF_{6}}$$
$$\mathrm{Cr(s)\:+\:2HCl(aq)\:\rightarrow\:Cr^{2+}(aq)\:+\:2Cl^{-}(aq)\:+\:H_{2}(g)}$$
与硫酸的反应表示为:
$$\mathrm{Cr\:+\:H_{2}SO_{4}\:\rightarrow\:CrSO_{4}\:+\:H_{2}}$$
铬中毒的主要症状
以任何形式接触这种金属都可能导致多种疾病。所有疾病都伴随着恶心、呕吐和眩晕等必要症状。此外,在这种类型的疾病中也观察到发烧和肌肉痉挛。这种类型疾病的症状严重程度可能是不同慢性症状(如肾衰竭、肝损伤和呼吸道不适)的主要原因。这种金属引起的常见疾病是肺癌,甚至肾脏和肝脏也受到这种金属反应的严重影响。
结论
它通过立即产生一层对氧气不透过的薄氧化层来保护金属主体。这种金属最重要的特性是它不会生锈,因此这些颗粒对电镀非常有帮助。由于这种优异的耐腐蚀性和硬度,这种特殊金属具有很高的金属价值。
常见问题
1. 铬属于哪个族?
在元素周期表中,铬属于第6族,周期为第4周期,分属于d区。纯净状态下,这种金属外观呈银白色,光泽度高,坚硬,适用于电镀。
2. 铬中包含哪些常见化合物?
在铬中,包含一些常见的化合物,例如铬酸钠、铬酸钾和重铬酸钾。此外,重铬酸铵和三氧化铬也包含在铬的化合物中。
3. 由于铬而产生的健康危害有哪些?
由于铬可能具有毒性,因此它会在人体内产生不同类型的健康危害。溃疡、皮炎和过敏性皮肤反应可能是由于这种金属引起的。
4. 使用铬之前可以采取哪些预防措施?
它是比铁、钨和钛更硬、更坚固的材料之一。如果处理不当,它通常会碎成小块并容易碎裂。Cr元素最常见的特性是极易脆。


 数据结构
数据结构 网络
网络 关系型数据库管理系统
关系型数据库管理系统 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 编程
C 编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP