一个原子具有电子层排布 2, 8, 7。
(a) 这个元素的原子序数是多少?
(b) 它在化学性质上与下列哪个元素相似?
(元素的原子序数已给出括号中)。
N (7), F (9), P (15), Ar (18)
(a) 一个原子具有电子层排布 2, 8, 7。因此,其原子序数为 2+8+7=17。氯的原子序数为 17。
(b) 氯与氟,F (9)相似,其电子层排布为 2,7。氯和氟在其外层电子壳层中都具有 7 个电子,因此它们是相似的。
[额外信息:
元素周期表: 元素周期表是所有化学元素的表格显示,按其原子序数、电子层排布和重复出现的化学性质进行排列。
它显示了已知元素的名称、原子序数、符号和原子量。它是解决化学问题的绝佳工具。
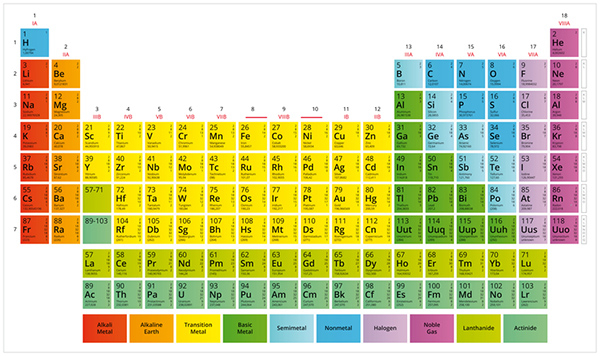
元素周期表很重要,因为它被组织成在一个参考中提供大量关于元素及其相互关系的信息。该表可用于预测所有元素的性质,甚至那些尚未发现的元素。]
- 相关文章
- 某元素的原子具有电子层排布 2, 8, 7。它在化学性质上与下列哪个元素相似?N (7)P (15)Na (11)F (9)
- 某元素的原子具有电子层排布 2, 8, 8, 2。(a) 该元素的原子序数是多少?(b) 它在化学性质上与下列哪个元素相似?(元素的原子序数已给出括号中):He (2); O (8); Mg (12); K (19) 说明你的选择理由。
- 一个原子具有电子结构 2, 7。(a) 该原子的原子序数是多少?(b) 它在化学性质上与下列哪个元素相似?7N, 15P, 17Cl, 18Ar (c) 为什么你认为它会相似?
- 下列哪个元素会形成酸性氧化物?(a) 原子序数为 7 的元素(b) 原子序数为 3 的元素(c) 原子序数为 12 的元素(d) 原子序数为 19 的元素
- 氮(原子序数 7)和磷(原子序数 15)属于元素周期表中的第 15 族。写出这两种元素的电子层排布。哪种元素的电负性更强?为什么?
- 如果已知元素的电子层排布,如何确定该元素的化合价?原子序数为 9 的元素的化合价是多少?
- 一个具有 8 个质子和 7 个中子的原子,其质量数和原子序数是多少?
- 某元素的原子具有电子层排布 2, 8, 2。它属于哪一族?第 4 族第 6 族第 3 族第 2 族
- 氯的电子层排布是(a) 2, 7 (b) 2, 8, 8, 7(c) 2, 8, 7 (d) 2, 7, 8。
- 某元素 X 的原子在其 M 层具有 7 个电子。(a) 写出元素 X 的电子层排布。(b) 元素 X 的原子序数是多少?(c) 它是金属还是非金属?(d) 元素 X 的原子将形成哪种离子?写出形成的离子的符号。(e) 元素 X 可能是什么?
- 某元素 X 的原子序数为 16。(a) 写下 X 的电子层排布。(b) X 的化合价是多少?
- (a) 如果已知元素的电子层排布,如何确定该元素的化合价?确定原子序数为 9 的元素的化合价。(b) 下面是一些现代元素周期表中的元素。元素的原子序数已给出括号中:A(4), B(9), C(14), D(19), E(20)(i) 利用电子层排布,找出上述元素中哪一个在其最外层电子壳层中只有一个电子。(ii) 哪两个元素属于同一族?说明你的理由。(iii) 上述元素中,属于第四周期的元素中,哪个元素的原子半径更大,为什么?
- (a) 描述汤姆逊的原子模型。汤姆逊的原子模型中不存在哪种亚原子粒子?(b) 某元素的质量数为 18。它包含 7 个电子。它的质子和中子数是多少?该元素的原子序数是多少?
- 某元素 Z 的电子层排布为 2, 8, 8。(a) 该元素的原子序数是多少?(b) 说明元素 Z 是金属还是非金属。(c) 元素 Z 的原子将形成哪种离子(如果有)?为什么?(d) 该元素的原子的最外层电子壳层有什么特殊之处?(e) 给出元素 Z 的名称和符号。(f) Z 属于哪一族元素?
- 一个原子的原子核有 5 个质子和 6 个中子。它的 (a) 原子序数,(b) 质量数,(c) 电子数,以及 (d) 每个原子的价电子数是多少?




 数据结构
数据结构 网络
网络 关系型数据库管理系统
关系型数据库管理系统 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 语言编程
C 语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP