胺的物理性质
介绍
胺是一类化合物,其物理性质与其与碳原子的连接方式有关。这种化合物的结构与氨非常相似。根据氨分子中氢原子被取代的程度,可以形成四种不同的胺。
什么是胺?
胺是一类具有独特性质的化合物。胺既是分子,也是有机化学中常见的官能团,其分子中含有孤对电子的碱性氮原子。胺通常被认为是氨的衍生物,其中一个或多个氢原子被烷基或芳基取代。一些重要的胺包括氨基酸、生物胺、三甲胺和苯胺。自然界中主要存在三种胺,分别为伯胺、仲胺和叔胺。分类是根据氨分子中被取代的氢原子数量进行的。
图1:胺
胺的分类
胺的分类主要是根据氨分子中被取代的氢原子数量进行的。以下是不同类型的胺:
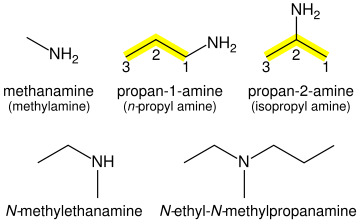
图2:胺的分类
Fvasconcellos 20:17, 8 January 2008 (UTC)。原始图像由 DrBob contribs)。, IUPAC-amine, CC BY-SA 3.0
伯胺
如果氨分子中的一个氢原子被烷基或芳基取代,则称为伯胺。由于这种胺在氮原子上只有一个取代基,因此以取代基为前缀命名。也称为1°胺。这种胺是在第一阶段形成盐(例如溴化铵)时产生的。
它类似于溴化铵,但是铵离子中的一个氢原子被乙基取代。氨从乙基铵离子中释放出氢原子,产生伯胺。
仲胺
使用两个不同的有机取代基取代氨分子中的氢原子,产生仲胺。氨从二甲基铵离子中释放出氢离子,留下仲胺,也称为二乙胺。
叔胺
当特定的有机化合物取代所有氢原子时,就会产生这种胺。它可以属于烷基或芳基。它是通过氨从三乙基铵离子中释放出氢离子而产生的,剩余的为叔胺,称为三乙胺。叔胺具有三个与氮原子相连的烷基。
环状胺
还有一种胺,其中氮原子包含在环状结构中,从而产生仲胺或叔胺。
胺的结构
根据胺的组成,氮原子的每个sp³杂化轨道都与氢原子或碳原子的轨道重叠。每个胺在氮原子的第四个轨道上都有一对未共享的电子。

图3:胺的结构
Kes47 (?), Primary-amine-2D-general, 标记为公共领域,更多详细信息请参见维基共享资源
由于存在未共享的电子对,C-N-E(其中E代表碳或氢)形成的角度小于109.5°。三甲胺的偏差角度略低,为108°。
胺的物理性质
以下是胺的一些性质:
低级脂肪胺以气态存在。
含有多个碳原子的伯胺在室温下为液体。
低级脂肪胺可以与水分子形成氢键,使其溶于水。
疏水性烷基链的增大增加了胺的摩尔质量。
伯胺的分子间缔合比仲胺强,叔胺没有分子间缔合。
伯胺的沸点最高,叔胺的沸点最低。
胺的用途
以下是胺的一些用途:
胺用于生产偶氮染料。
它们广泛用于生产用于保护农作物和食品的化学品。
胺也有助于生产药品。吗啡和度冷丁是有效的止痛药。
胺可用作杀虫剂。
胺有助于皮革鞣制。
甲基苯丙胺和苯丙胺被认为是娱乐性毒品。
它们也存在于个人护理产品中。
胺以乙醇胺的形式广泛存在于全球市场。
结论
胺是一种非常常见的物质,广泛用于各种用途。胺是由氨通过用其他有机化合物取代氢原子而制成的。主要存在三种类型的胺,它们具有各自独特的性质。胺主要存在于麻醉剂和药品中。其易溶于水等性质使其在不同行业中非常有用。
常见问题
Q1. 胺易燃吗?
A1. 一般来说,胺的沸点较高,伯胺的沸点最高。这些物质是可燃的,但在室温下并不容易燃烧。
Q2. 胺的化学性质是什么?
A2. 胺是有机化合物,含有一个或多个氮原子,其结构通常取决于这些原子。胺也与氨的结构相似,但胺还具有取决于碳原子的额外性质。
Q3. 胺在哪里使用?
A3. 胺主要用于麻醉品和医药行业。借助这种化合物可以生产各种药物。胺也用于生产用于水净化的化学品。这些产品也存在于化妆品和护理产品中。胺也存在于用于保护化学品的安全化学品中。


 数据结构
数据结构 网络
网络 关系数据库管理系统 (RDBMS)
关系数据库管理系统 (RDBMS) 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C语言编程
C语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP