气体示例
简介
气体的例子如下:氧气、氢气、氦气等。气体是物质四种状态之一,这并不是一个新的现象。气体由分子组成,分子由单个原子组成。这些原子可以是相同的,也可以是不同的,从而分别形成元素和化合物。与气体相关的性质介于液态和等离子态之间。
所有气体的物理特性和成分都基于它们之间的分子间力和分子间空间。与液体和固体相比,由于分子间分离对分子间力的支配作用,气体之间存在非常大的空间。这就是气体不能像固体和液体那样被固定或塑形的原因。所有这些与气体相关的性质都受温度和压力的影响,在气体的情况下,温度和压力成反比。
图 1:气体分子的描述
气体示例
气体存在于不同的类型,并且有很多例子。气体的例子可以在不同的上下文中进行分类。气体例子分类的两个类别是 -
同核分子气体
异核分子气体
同核分子气体
顾名思义,同核气体是指仅由一种类型的原子组成,并且由相同的元素组成的气体。这些也称为元素气体。同核气体在标准温度和压力条件下存在。由于压力和温度的变化,气体可以改变其组成。根据所涉及的原子数量,同核分子气体分为三种类型。
单原子气体
双原子气体
三原子气体
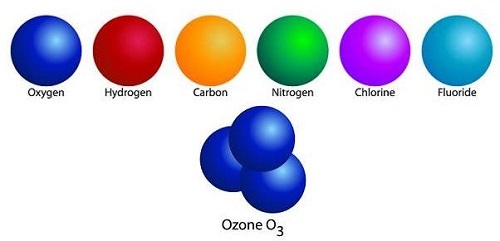
图 2:同核气体的示例
单原子气体
单原子气体是由单个原子组成的同核气体。由于没有旋转和振动常数,并且由于涉及单个元素,因此单原子气体在热力学性质方面具有非常简单的组成。单原子气体的常见例子是稀有气体和某些金属的蒸汽。它们如下 -
氦 (He)
氖 (Ne)
氩 (Ar)
氪 (Kr)
氙 (Xe)
氡 (Rn)
钠蒸汽 (Na)
钾蒸汽 (K)
双原子气体
从名称可以看出,双原子气体涉及两个相同或不同元素的键合。在同核气体的类别中,这些被认为是同核双原子气体。双原子气体通常由非金属组成,并通过共价键形成。共价键是一种化学键类型,涉及电子的共享。
在同核双原子气体的情况下,形成的共价化合物或气体是非极性共价气体。这是因为相同的原子彼此键合,不涉及电荷差异,因此不存在净偶极矩。与单原子气体不同,这些气体并不简单,温度和压力的变化也会导致其组成的变化。双原子气体不被认为是良好的导电体或导热体。同核双原子气体的例子有 -
氢气 $\mathrm{(H_2)}$
氮气 $\mathrm{(N_2)}$
氧气 $\mathrm{(O_2)}$
氟气 $\mathrm{(F_2)}$
氯气 $\mathrm{(Cl_2)}$
溴气 $\mathrm{(Br_2)}$
三原子气体
顾名思义,三原子气体包括三个原子之间的键合。定义是灵活的,并且像双原子气体一样,这些气体也可能是同核的和异核的。这里只讨论同核部分。众所周知,最常见的同核三原子气体包含三个氧原子。还有许多其他同核三原子气体,但这些气体不稳定,最终会分解成阳离子或其他稳定的产物。因此,稳定的同核三原子气体是 -
$\mathrm{臭氧\:(O_3)}$
异核分子气体
异核气体由不同原子的分子组成。与同核分子一样,这些也分为单原子、双原子和三原子异核气体。异核气体也称为混合气体,因为它们由不同类型的原子组成。异核气体中的键合可以是共价键、电价键或配位键。根据异核气体中键合的多样性和所涉及的原子类型,将其分类为有机气体或无机气体。下面列出了各种类别的异核气体的各种例子 -
空气(氧气、二氧化碳、氮气和其他气体的组合)
二氧化碳 $\mathrm{(CO_2)}$
一氧化碳 $\mathrm{(CO)}$
乙炔 $\mathrm{(C_2H_2)}$
丁烷 $\mathrm{(C_4H_{10})}$
二甲醚 $\mathrm{(C_2H_6O)}$
氨气 $\mathrm{(NH_3)}$
硫化氢 $\mathrm{(H_2S)}$
甲烷或天然气 $\mathrm{(CH_4)}$
一氧化二氮 $\mathrm{(N_2O)}$
乙烷 $\mathrm{(C_2H_6)}$ 等等。
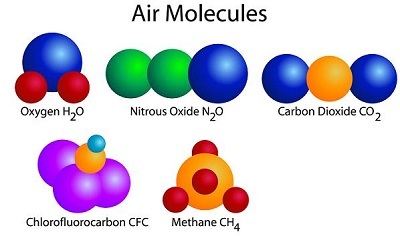
图 3:异核气体的示例
有毒气体及其例子
某些气体不适合吸入,可能对人体有害甚至致命。意外吸入有毒气体或轻微接触都可能导致人死亡,在某些情况下,它可能使人感到头晕和恶心。在重工业或化工厂工作的人员应了解有毒气体,并在工作时采取必要的措施。下面讨论了有毒气体示例的列表 -
氯乙烯 $\mathrm{(C_2H_3Cl)}$
三氯硅烷 $\mathrm{(SiHCl_3)}$
三甲胺 $\mathrm{(C_3H_9N)}$
二氧化硫 $\mathrm{(SO_2)}$
臭氧 $\mathrm{(O_3)}$
四氧化锇 $\mathrm{(OsO_4)}$
氯化氢 $\mathrm{(HCl)}$
硫化氢 $\mathrm{(H_2S)}$
磷化氢 $\mathrm{(PH_3)}$
光气 $\mathrm{(COC_{l2})}$
六氟化钨 $\mathrm{(WF_6)}$
甲醛 $\mathrm{(CH_2O)}$
各种气体的应用
有各种各样的气体示例在维持地球上的生命及其运作方面发挥着重要作用。气体种类繁多,可以属于不同的类别。气体示例的列表是无穷无尽的。与气体相关的物理和化学性质及其行为使其在各种应用中都非常有用。气体存在于各种环境和条件的使用中。
讨论了气体的自然用途,这些用途在地球上扮演着生存基本要素的角色。空气是呼吸所必需的。各种生物地球化学循环只有在气体存在的情况下才能维持生态系统的平衡。作物的生长和粮食生产的维持是由含氮量高的气体实现的。例如,豆科植物的生长只有通过将大气中的氮气转化为硝酸盐才有可能,而硝酸盐又被细菌进一步利用以促进植物的正常生长。
在工业中,气体以商业规模生产以帮助不同的过程和部门。这些气体被称为工业气体。有机和无机工业气体都用于各种工业过程中,例如钢铁制造、石油化工分析、半导体行业、医疗行业、化肥生产、H2 分析行业等。
结论
简而言之,气体是我们生活和地球上生命顺利运行的组成部分。它不仅对人类生命的存在具有重要意义,而且对维持所需的生态平衡和可持续性也至关重要。在商业上,气体对各种部门和行业来说都是一项福音。尽管我们无法因其特性而将其封闭,但其存在和用途是不可否认的。
常见问题
Q1. 什么是气体定律?简要解释所有气体定律。
答:气体定律是一组定律,它们根据气体体积、压力、温度和气体摩尔数的变化来观察气体不同的行为变化。四条气体定律建立了所有导致气体行为改变的因素之间的关系。这些定律是 -
波义耳定律:建立压力和体积之间的关系。
盖-吕萨克定律:展示压力和温度之间的关系。
查理定律:定义体积和温度之间的关系
阿伏伽德罗定律:定义体积和量之间的关系
Q2. 简要讨论理想气体。
答:理想气体是一个理论概念,它在标准温度和压力条件下工作,在这些条件下,气体不受外部环境条件的影响。理想气体遵循理想气体方程
$$\mathrm{PV = nRT}$$
在现实世界中,没有气体是理想气体,但在某些标准压力和温度条件下,稀有气体、N2 和 O2 在一段时间内表现出类似理想气体的行为。
Q3. 气体上的压力是如何产生的?
答:气体压力是由气体分子彼此碰撞以及与容器壁碰撞产生的。这些碰撞传递少量力并产生动量。动量通常取决于速度,而速度又取决于温度升高。因此,温度升高越多,速度和动量就越大,气体施加的压力就越大。这种压力可用于各种化学和热力学过程。
Q4. 气体在光化学中起什么作用?
答:气体存在于大气中,因此,所有关于气体的研究都归类于大气化学。另一方面,光化学是利用光进行各种反应,而这些反应也发生在大气条件下。因此,气体有助于光化学反应。例如,在臭氧和氯氟烃中观察到链式反应。在电离层,气体通常由于紫外线或宇宙辐射而转化为离子,这些辐射足够强以去除电子。


 数据结构
数据结构 网络
网络 关系型数据库管理系统
关系型数据库管理系统 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 编程
C 编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP