
化学 - 碳
简介
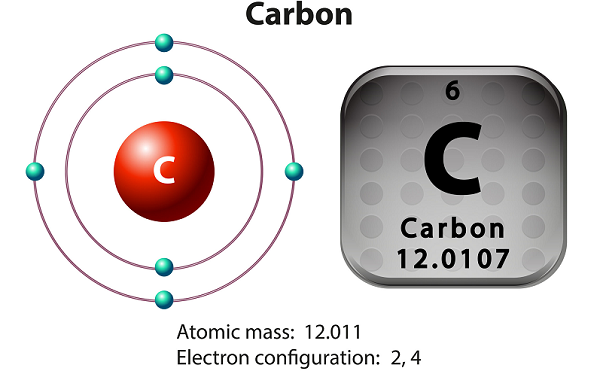
碳是一种非金属四价元素。
四价意味着 - 碳提供四个电子形成共价化学键。
碳有三种自然存在的同位素 - 即12C、13C和14C。
其中,12C和13C是稳定的,但14C是放射性同位素。14C的半衰期约为5730年。
碳的显著特征
碳的物理性质很大程度上取决于其同素异形体。
碳的主要同素异形体是石墨、金刚石和无定形碳。
石墨是不透明的、黑色的、非常柔软的;因此,它用于在纸上留下痕迹。
金刚石非常坚硬(自然界中最硬的物质)且透明。
石墨是良好的导电体。
金刚石是不良导电体。
碳很可能在所有元素中具有最高的升华点。
碳的分布
就质量而言,碳是宇宙中第四丰富的化学元素(仅次于氢、氦和氧)。
碳在太阳、恒星、彗星以及大多数行星的大气中都大量存在。
碳存在于地球大气中并溶解在水中。
碳氢化合物,如煤、石油和天然气,都含有碳。
碳也存在于甲烷水合物中,甲烷水合物存在于极地地区和海底。
一些富含碳的岩石是煤、石灰石、白云石等。
煤富含碳;因此,它是最大的矿物碳商业来源。
煤约占化石燃料总量的4000亿吨或80%。
碳的化合物
以下是碳的主要化合物:
氰- CN2
氰化氢- HCN
氰胺- CN2H2
异氰酸- HNCO
氰化氯- CNCl
氯磺酰异氰酸酯- CNClO3S
氰尿酰氯- NCCl3
二硫化碳- CS2
硫化羰- OCS
一硫化碳- CS
碳的用途
根据同素异形体,碳被用于各种应用。
碳是生命中最基本的元素之一,没有它,我们就无法想象地球上的生命。
化石燃料,如甲烷气体和原油(石油)、煤等,在日常生活中被使用。
石墨与粘土混合,用于制造铅笔芯。
木炭也用作艺术作品中的绘画材料、炼铁、烧烤等。
金刚石通常用于珠宝。
工业用金刚石用于切割、钻孔和抛光工具,用于加工金属和石头。
化石碳氢化合物和碳纤维用于制造塑料。
广告