酮的制备
引言
羰基 (𝑪 = 𝑶) 存在于称为酮的化学分子中。酮是反应迅速的化学物质。酮和醛关系密切,但酮的反应活性比醛弱。
酮的不均匀电荷分布导致其极性特征。酮是许多构建块的基础。它可以用于制造纺织品、溶剂(用于制造炸药)、油漆、清漆等。酮还用于水力压裂剂的处理、修复和染色。实验室和工业规模上经常使用多种酮的制备方法。
什么是酮?
酮可以被认为是有机化合物,含有羰基,即一个碳原子与一个氧原子连接,其余键与烃基相连。在酮的情况下,两个 R 基团连接到羰基(𝑪 = 𝑶)。酮基存在于消炎药中。
酮的结构
在化学中,酮是一个官能团,其化学式为$\mathrm{R_{2}C\:=\:0}$。酮中的羰基碳通常被称为“𝒔𝒑𝟐杂化”。酮围绕酮羰基碳呈三角平面形,具有约120°的碳-碳-碳键角和碳-碳-氧键角。与醛不同,酮分子中羰基 (𝑪𝑶) 连接到碳骨架中的两个碳原子。

酮的反应
酮被认为是化学中最高反应活性的物质之一。然而,酮比醛不那么活泼和反应性。考虑到羰基是所有化学反应的基础,酮和醛是相似的。酮的极性特征是由其不均匀的电荷分布引起的。不均匀的排列导致碳原子上带正电荷。以下是酮的一些重要反应:
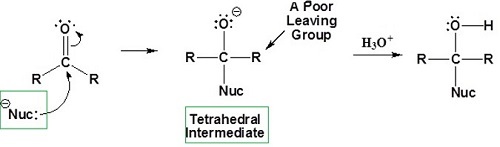
亲核试剂对酮羰基的进攻。 −
亲核试剂加到羰基的亲电碳上。随后进行质子化,形成𝑂 − 𝐻键。
酮与氨或1°胺反应可以生成亚胺。 −
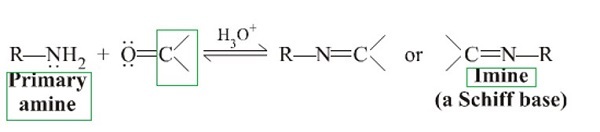
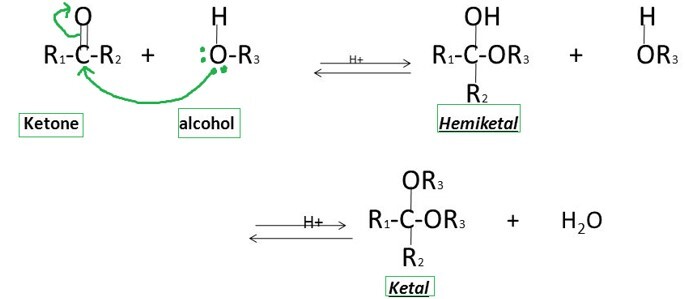
与醇的反应
当酮与醇或醇盐反应时,会生成半缩酮或其相应的碱。二醇转化为缩酮。此反应用于保护酮。
酮与强氧化剂反应生成羧酸。 −

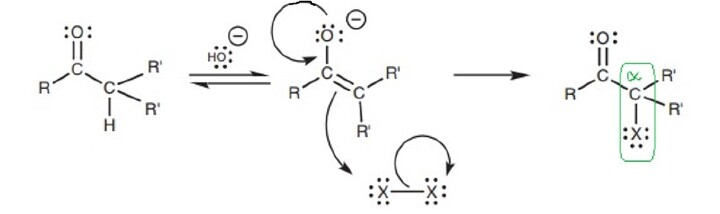
与卤素的反应 −
烯醇作为介质,将酮转化为α-卤代酮。
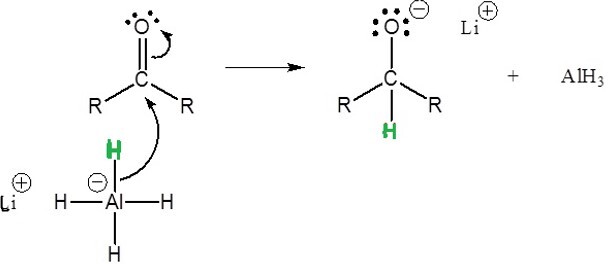
与还原剂的反应 −
酮与还原剂如$\mathrm{LiAlH_{4}}$反应生成仲醇。

酮的鉴定
通过化学名称 − 仅通过其化学名称即可鉴定酮。化学名称末尾的“one”后缀表示酮的存在。
通过溶解度 − 必须研究溶液在水中的溶解度和沸点,根据其物理特性来确定酮。如果它是关键成分,则其在水中的溶解度和沸点都将非常重要。
通过光谱 − 酮和醛在接近1700 𝒄𝒎−𝟏的红外波长处强烈吸收。根据组成,13𝐶 𝑁𝑀𝑅谱显示信号略微向下场移动到200 ppm。
有机试剂 − 酮在2,4-二硝基苯肼试验(布拉迪试验)中呈阳性结果,在费林溶液或托伦试剂试验中呈阴性结果。
酮的制备
在化学实验室和工业规模上,经常使用多种酮的制备方法。以下是其中一些方法:
由腈制备酮
通过这种方法,可以使用格氏试剂作用于腈来制备酮。格氏试剂将靶向腈中的亲电碳中心以生成亚胺盐。生成的溶液必须经过水解才能得到酮作为产物。

格氏试剂与腈在水性酸中反应,会生成酮,同时产生氨和镁盐作为副产物。
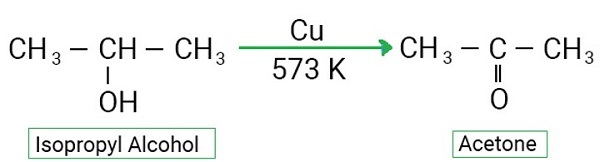
通过醇的脱氢制备酮
如果从相应的醇分子中去除一个氢分子,则醇会发生脱氢反应。在氧化过程中,C − O和O − H强的键被还原为纯粹的C = O键。因此,需要仲醇的脱氢来形成酮。
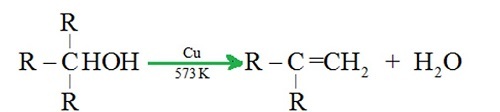
然而,对于叔醇,由于在这种情况下不存在α-氢,因此应在有机物的氧化之后用脱水过程代替脱氢过程。
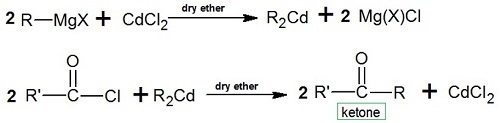
由酰氯制备酮
一旦格氏试剂与酰氯反应后暴露于强金属卤化物中,酮就会合成。例如,当氯化镉被迫与敏感试剂反应时,会产生二烷基镉。此后产生的产物准备好与酰氯反应生成酮。
反应 −
该过程的机理如下所示
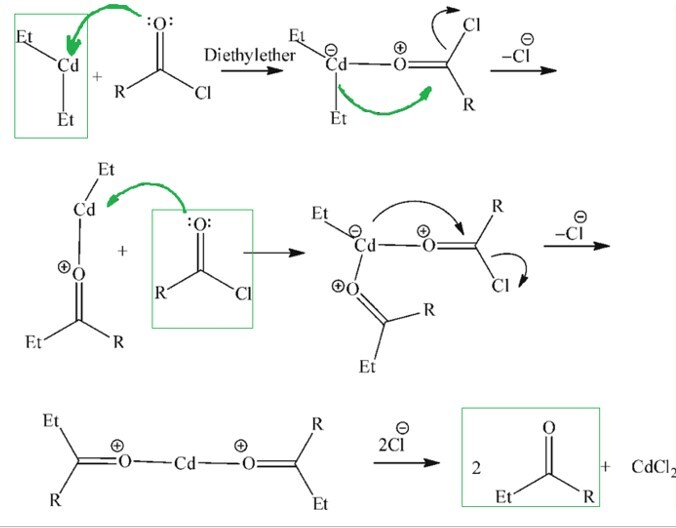
由苯和取代苯制备酮
苯及其取代形式易于生成芳香酮。这被认为是化学中制备芳香酮最有效的方法。该方法包括用酰氯处理苯以生成酮。只有催化剂(例如路易斯酸,如用酰氯处理的苯$\mathrm{AlCl_{3}}$)的存在才能使这种反应成为可能。
反应 −

该过程的机理如下所示
步骤1 − 亲电试剂的形成。
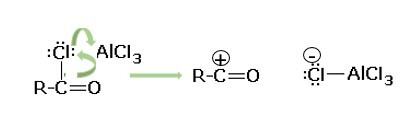
步骤2 − 亲电试剂对苯环的进攻。
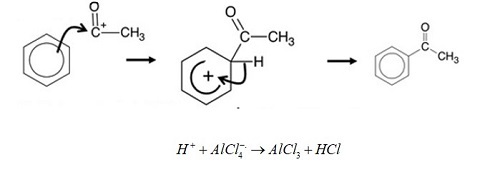
结论
酮的标准式为𝑹(𝑪 = 𝑶)𝑹′,其中 R 和 R' 可以是烷基或芳基。根据其取代基,它们分为两种类型:酮的对称形式和不对称形式。酮可以通过多种方法大量制备,并在实验室中制备。烃、醇和其他化合物经常发生氧化反应生成酮。
常见问题解答
1. 哪种方法不使用烷基腈来制备酮?
烷基腈不能在酸中水解以释放酮。
2. 什么可以还原酮?
几种还原剂可以还原醛和酮。两种主要的还原剂是硼氢化钠和氢化铝锂。
3. 为什么酮不氧化?
酮不易氧化,因为它们的羰基不含氢原子。酮只能被非常强的氧化剂(如高锰酸钾溶液)氧化。
4. 为什么酮的反应速度比醛慢?
因为酮中的两个烷基显著降低了羰基碳的亲电性,比醛中的亲电性低,所以酮比醛活性低。
5. 为什么酮的沸点比醛高?
酮的沸点比异构醛略高。这是因为羰基碳被两个给电子基团包围,使其更极性。


 数据结构
数据结构 网络
网络 关系数据库管理系统 (RDBMS)
关系数据库管理系统 (RDBMS) 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C语言编程
C语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP