苯胺黄的制备
介绍
苯胺黄是偶氮苯的衍生物,呈橙色粉末状。它由 C. Mene 于 1861 年首次制备。1864 年,它作为第一个偶氮染料被商业化。它在水中微溶,可溶于乙醇、苯和油中。它是一种弱碱,与无机酸形成盐。
什么是苯胺黄?
苯胺黄也称为对氨基偶氮苯,通过偶氮染料的最简单的偶联反应获得。由于其对酸敏感的性质,这种染料没有工业意义。

图 1 - 苯胺的化学式
为了获得纯染料,通过将其溶解在四氯化碳溶剂中进行粗样品的重结晶。可以使用简单的石蕊试纸测试来识别苯胺黄。由于苯胺”呈碱性,因此它会将红色石蕊试纸变为蓝色。
苯胺黄的用途
下面讨论苯胺黄的用途:
它用于橡胶促进剂。
用作染料和中间体
用于除草剂和杀虫剂。
用于石油精炼和炸药
用于制药和制造炸药
苯胺的性质
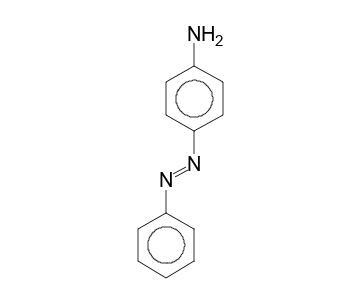
图 2 - 苯胺黄的分子结构
它是一种黄色油状液体,暴露在空气或光线下会变暗。它还具有胺的气味和灼烧的味道。它表现出弱碱性,并在无机酸存在下形成盐。苯胺黄的pH值为8.8。它是一个极性分子,充当氢键供体。其毒性会损害血红蛋白,使其无法携带氧气。
研究目的
目的是从苯重氮氯和苯胺制备苯胺黄。
苯胺黄生产理论
本研究提到了关于有效生产的一些有效理论。苯胺黄制备的第一阶段始于苯的形成
从苯胺制备重氮氯。为此,苯胺在酸存在下用亚硝酸钠处理。它产生苯重氮氯盐。然后将该盐与苯胺偶联以产生对氨基偶氮苯的黄色沉淀,也称为苯胺黄。它具有挥发性,并用作生产其他颜色的中间体。
制备过程的化学反应
下面讨论了苯胺黄制备中涉及的化学反应。
步骤 1
$$\mathrm{Ar\:-\:NH_{2}\:+\:NaNO_{2}\:+\:HCl\:\rightarrow\:Ar\:-\:N_{2}^{+}\:.\:Cl^{-}}$$
步骤 2
$$\mathrm{Ar\:-\:N_{2}^{+}.Cl\:+\:Ar\:-\:NH_{2}\:\rightarrow\:Ar\:-\:N\:=\:N\:-\:NH\:-\:Ar}$$
步骤 3
$$\mathrm{Ar\:-\:N\:=\:N\:-\:NH\:-\:Ar\:\rightarrow\:Ar\:-\:N\:=\:N\:-\:Ar\:-\:NH_{2}}$$
在初始阶段,苯胺”充当亲核试剂,因此与苯重氮氯$\mathrm{C_{6}H_{5}N_{2}^{-}Cl^{-}}$反应形成 C-N 键。在下一步中,它失去其 H+ 离子并导致偶氮染料。
所需材料
下面讨论了制备苯胺黄所需的材料:
苯胺
盐酸 (盐酸)
亚硝酸钠
冰醋酸
本生灯
蒸馏水
圆底烧瓶
烧杯
搅拌器
漏斗
水浴
锥形瓶
程序
下面讨论了制备苯胺黄的步骤:
取 10 毫升盐酸与 20 毫升水混合,然后在混合物中加入 4 毫升苯胺。
完全溶解混合物
将溶液在冰浴中冷却至约 5°C。
将 4 克亚硝酸钠加入水中并搅拌直至完全溶解
将此溶液与苯胺溶液混合以制备苯重氮氯溶液
加入 4 毫升盐酸并向苯重氮氯溶液中加入 4 毫升苯胺。这种偶联反应导致苯胺黄的形成
为了获得纯染料,通过将其溶解在四氯化碳溶剂中进行粗样品的重结晶。
形成纯黄色沉淀,称为苯胺黄,并将这种黄色沉淀通过布氏漏斗过滤并保存干燥。
注意事项
下面提到了此制备过程的注意事项:
不要触摸染料,因为它具有粘性。
实验温度应保持在 40° 至 50° 之间
实验的 pH 值必须在 4 到 5 之间。
粗样品必须用清水反复清洗
在进行此实验时,需要一些防护措施,例如实验服、手套和护目镜。硝基苯的还原是通过在酸性水溶液中使用铁屑进行的。
结论
实验温度不得超过 50℃,以避免爆炸。但是,由于其对酸的敏感性,它没有工业意义。苯胺黄是在酸性介质中苯重氮氯与苯胺偶联产生的。从苯胺合成苯重氮氯是苯胺黄形成的第一步。随后,通过苯重氮氯和苯胺的偶联产生偶氮染料。
常见问题解答
1. 从化学上区分苯酚和苯胺?
通过简单的石蕊试纸测试可以识别它。由于苯胺呈碱性,因此它会将红色石蕊试纸变为蓝色,而苯酚呈弱酸性,因此它会将蓝色石蕊试纸变为红色。
2. 苯胺是比氨弱的碱吗?
苯胺是比氨弱的碱,因为苯环在苯胺中的共振效应使得氮原子上孤对电子的可用性降低。
3. 重氮化是什么意思?
它是亚硝酸与无机酸反应生成重氮盐作为产物的反应过程
4. 苯胺黄是染料吗?
它是一种黄色偶氮染料和芳香胺,也呈橙色粉末状。


 数据结构
数据结构 网络
网络 关系型数据库管理系统
关系型数据库管理系统 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 编程
C 编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP