草酸标准溶液的制备
介绍
草酸的标准单位溶液在特定体积的溶剂中用作基准标准溶液。它被制备用于作为基准标准物质。
什么是草酸?
草酸是一种有机产物,分子式为“2H2O4。其 IUPAC 名称为乙二酸。该产物由二羧酸组成。它是一种弱酸,以白色结晶形式存在。
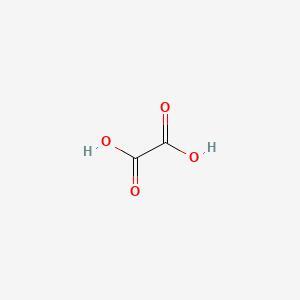
图 1 - 草酸
草酸在水中形成无色溶液。草酸的分子量为 90.03g/mol。该产物比乙酸具有更强的还原性。富含草酸的食物对健康有益。然而,它对人体也有一些有害影响。该产物可能导致肾结石和许多其他复杂问题。自然界中,该产物以二水合物形式存在,如 $\mathrm{C_{2}H_{2}O_{4}.H_{2}O}$。
目的
本实验旨在制备 M/10 或 0.1M 的草酸标准溶液。
理论
水合草酸在自然界中以 $\mathrm{C_{2}H_{2}O_{4}.H_{2}O}$ 的分子式存在,质量为 126 g/mol。M/10 草酸标准溶液的制备是通过将 12.6g 草酸/升混合制得。需要 3.15g 草酸晶体与水混合,制备 250 mL 的溶液。
所需材料
以下是实验所需的材料:
化学天平
表面皿
砝码盒
250mL 烧杯
玻璃棒
250mL 容量瓶
洗瓶
称量管
草酸
漏斗
漏斗架
蒸馏水
步骤
实验中遵循以下过程:
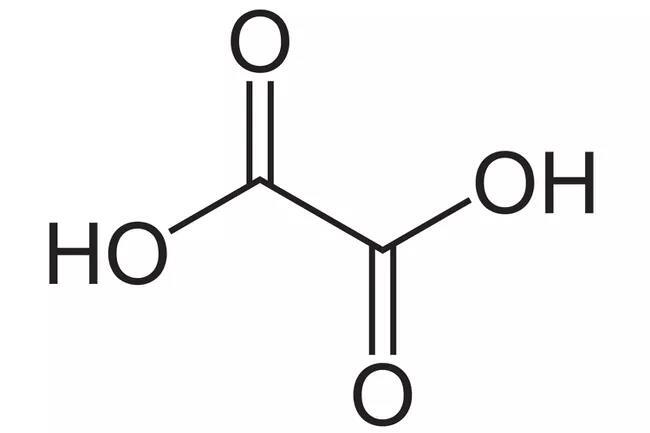
图 2 - 草酸的分子结构
用蒸馏水清洗表面皿并干燥后,将其用于反应。
应称量表面皿的重量,并将数据记录在笔记本中。
精确称量 3.15g 草酸,并将数据记录在笔记本中。
使用漏斗,将草酸从表面皿小心地转移到量筒中。
清洗表面皿以去除粘在里面的不需要的颗粒。此过程借助洗瓶完成。蒸馏水的体积绝不能超过 50mL。
需要彻底清洗漏斗,借助洗瓶将多余的颗粒转移到量筒中。少量水用于清洗漏斗。蒸馏水再次不应超过 50mL 的水平。
用蒸馏水冲洗漏斗,将溶液转移到容量瓶中。
打开容量瓶,直到草酸溶解。
借助洗瓶,在容量瓶中加入适量的蒸馏水。水位始终应低于瓶上的刻度线。
最后几毫升蒸馏水应滴加到容量瓶中,直到水位达到刻度线。
在烧瓶口加塞,然后小心摇晃烧瓶,使溶液均匀。应得到 M/10 草酸溶液。
观察和结果
实验的观察结果和结果如下:
| 表面皿的重量 | W1g |
|---|---|
| 表面皿 + 草酸的重量 | W1 + 3.15g |
| 草酸的重量 | 3.15g |
| 蒸馏水的体积 | 250cm3 |
表 1 - 实验观察结果
结果
得到 250cm3 的 M/10 草酸溶液。
注意事项
应遵循某些注意事项:
正确称量草酸晶体的重量。砝码应为 $\mathrm{2g\:+\:1g\:+\:100mg\:+\:50mg}$。
应将表面皿清洗并干燥,以便可以将每一粒草酸晶体倒出来。
应使用移液管添加额外的几滴蒸馏水,以避免添加过量的水。
滴定过程中,应在约 60°C -70°C 加热烧瓶,并在烧瓶中加入几滴稀 $\mathrm{H_{2}SO_{4}}$ 溶液。
结论
草酸是一种相当丰富的产物,存在于日常生活中食用的不同食物中。它也以最简单的二羧酸形式出现。草酸通常为白色,以八面体晶体形式获得。可以通过遵循某些预防措施在实验室中合成这种化合物。它通常以二水合物形式存在。
常见问题
1. 草酸是如何得名的?
早期从酢浆草属植物的花朵中分离出草酸的研究人员。这些花通常被称为酢浆草。
2. 草酸有哪些有害影响?
这种化合物存在于各种食品中,当该产物接触皮肤时,可能对人类有害。过量摄入该产物可能导致致命后果。
3. 标准溶液是什么意思?
标准溶液是指浓度的溶液。通过混合特定体积的溶剂来制备标准溶液。


 数据结构
数据结构 网络
网络 关系数据库管理系统
关系数据库管理系统 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C语言编程
C语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP