什么是电解? - 定义、原理和过程
什么是电解?
电解过程可以用多种方式定义:
利用直流电刺激非自发化学反应的技术称为**电解**。
换句话说,通过离子物质传递电流将其分解成简单物质的过程称为**电解**。
或者,**电解**是基于电能可以产生化学变化的事实,即它可以导致化学反应发生的过程。
电解原理
电解的原理基于“**电解质**”这一术语。电解质是一种含有自由离子的物质,使该物质具有导电性。通常,电解质是离子溶液,但熔融电解质和固体电解质也存在。
在自然界中,电解质的原子紧密结合在一起,但当溶解时,这种键会变弱,电解质的分子会分裂成两种类型的离子,即阳离子(带正电的离子)和阴离子(带负电的离子),在溶液中自由移动。
现在,如果将两个电极浸入电解质中并连接到直流电源。然后,溶液中自由移动的阳离子会被阴极吸引,而溶液中自由移动的阴离子会被阳极吸引。
电解过程
为了理解电解过程,我们考虑以下示例。
考虑一个盛满水的坩埚,其中浸入两个电极,即阳极和阴极,这些电极由直流电源供电。电解过程的装置如图所示。
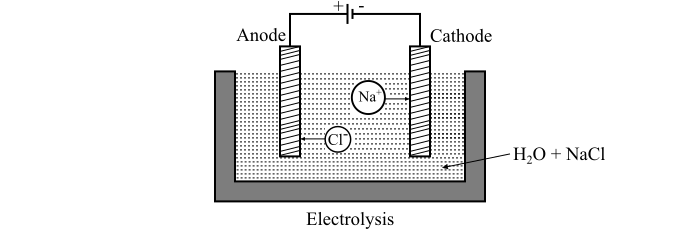
现在,当氯化钠(NaCl)盐溶解在水中时,它会分解成带正电的Na+离子以及带负电的Cl−离子,在溶液中自由移动。由于电极连接到直流电源,因此带正电的Na+离子向阴极移动,而带负电的Cl−离子向阳极移动。
到达阴极后,每个带正电的钠(Na+)离子从阴极获取一个电子并形成钠金属。类似地,每个带负电的氯离子会将一个电子传递给阳极,并停止成为阴离子。现在,沉积在阴极上的钠金属与水发生反应,并释放出氧气和氯化氢,即:
$$\mathrm{4Cl\: +\: 2H_{2}O\to 4HCL\: +\: O_{2}} $$
这种从水中氯化钠(NaCl)中在阴极沉积钠的过程称为**电解**。
现在,如果阴极由钠制成,则氯化氢会再次与钠金属反应,形成氯化钠并释放出氢气。此过程也可以用以下化学反应表示。
$$\mathrm{2HCl\: +\: 2Na\to 2NaCl+H_{2}} $$
电解的应用
电解被广泛用于:
精炼金属,如金、银、铜等。
从矿石中提取纯金属,如铝、铜、锌等。
各种电沉积过程,如电镀、电铸等。
制造各种化学品。


 数据结构
数据结构 网络
网络 关系型数据库管理系统
关系型数据库管理系统 操作系统
操作系统 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C语言编程
C语言编程 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP